
A��B��C��D��E��F�������ʵ���ɫ��Ӧ��Ϊ��ɫ�� A��B��C��D�����ᷴӦ������E������B������—�ֿ�ȼ�����壻��C��D������—����ɫ��ζ������H����������ʹ�����ʯ��ˮ����ǡ�D��A�ɷ�Ӧ����C��F��HҲ�ɷ�Ӧ����C����—����ɫ��ζ���塣
��ش��������⣺
��1��д��B��C�Ļ�ѧʽ��B��___________________; C��___________________;
��2��д��F��H2O��Ӧ�Ļ�ѧ����ʽ��__________________________________;
��3��д�����з�Ӧ�����ӷ���ʽ
��D��Һ+���_____________________________________________________;
��D��Һ+A��Һ��___________________________________________________;

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA���������ӵ���������ֵ������������ȷ����
A����������ķ�Ӧ�У�5.6g����ȫ��Ӧʧȥ�ĵ�����һ��Ϊ0.3NA
B��1mol 12C18O2�У�������������Ϊ22NA
C����״���£�11.2 LCO��N2��������к��еķ�������0.5NA
D�������£�pH=12��1L��ˮ�к��е�NH3��H2O��������0.01 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����IJ����Ǻ���һ�����һ���ˮƽ�ı�־��2SO2(g) + O2(g)  2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
2SO3(g)�ǹ�ҵ���������Ҫ��Ӧ֮һ��һ���¶��£��ڼס��ҡ��������ݻ���Ϊ2 L�ĺ����ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
| �� | �� | �� | ||
| ��ʼ���ʵ��� | n(SO2) / mol | 0.4 | 0.8 | 0.8 |
| n(O2) / mol | 0.24 | 0.24 | 0.48 | |
| SO2��ƽ��ת���� | 80% | ��1 | ��2 |
�����ж��У���ȷ����
A�����з�Ӧ��ƽ�ⳣ��С���� B��ƽ��ʱ������c(SO3)�Ǽ��е�2��
C�����¶��£�ƽ�ⳣ��ֵΪ400 D��ƽ��ʱ��SO2��ת���ʣ���1<80%<��2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A. Fe��������ȼ������FeCl2
B ��AlCl3��Һ��ε��뵽NaOH��Һ���Ȳ�����ɫ��������������ʧ
C�������л������ۼȿ��ù�����NaOH��Һ��Ҳ�����ù���FeCl3��ַ�Ӧ���˳�ȥ
D�������£�����Ʒ��Ũ�����Ũ���ᴦ����������ʴ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪�������������Ũ���ᷴӦ�ܷų��������ְ�����ͼ��������������ʵ�顣�������ڷֱ�װ�е���������ͬ��Һ�İ�ɫ����Ӧ—��ʱ���ͼ��ָ����λ��ɫ������ȷ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����˵����ȷ����( )
A��֬��������������±������������
B����Ȼ����������ˮú�������ڿ������������
C����ҵ�Ϸֱ����Ȼ�ԭ�����ȷֽⷨ�͵�ⷨұ��ͭ��þ����
D�����ǡ����ᱵ��ˮ�ֱ����ڷǵ���ʡ�ǿ����ʺ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Ҫ�Ľ���Ԫ��,��;���㡣
��1���������(K2FeO4)���к�ǿ�������ԣ���������ˮ�����Ի�������Ӱ��,�����dz�Ϊ����ɫ��ѧ���Լ�����ҵ�ϣ������������������KOH��Һ�Ʊ�K2FeO4���������ĵ缫��ӦʽΪ___________________��
��2��ij��Ч��ˮ������Fe(OH)SO4�ۺϵõ�����ҵ����FeSO4��NaNO2��ϡ����Ϊԭ�����Ʊ�Fe��OH��SO4����Ӧ����NO���ɣ���ѧ����ʽΪ�������� ��������
��3����֪�� ��Fe2O3(s)+3C(ʯī) = 2Fe(s)+3CO(g) ��H1 = + 489.0 kJ/mol
��C(ʯī)+CO2(g) = 2CO(g) ��H2 = + 172.5 kJ/mol
��¯���������з�������Ҫ��ӦΪ��
 Fe2O3(s)+ CO(g)
Fe2O3(s)+ CO(g) 
 Fe(s)+CO2(g) ��H = a kJ/mol,��a = kJ/mol��
Fe(s)+CO2(g) ��H = a kJ/mol,��a = kJ/mol��
��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����±���

��һ���ݻ�Ϊ10L���ܱ������У�1000��ʱ����Fe��Fe2O3��CO��CO2��1.0 mol����ʱv�� v��������ڡ��������ڡ���С�ڡ�)������l0 min����1000��ﵽƽ�⣬���ʱ�䷶Χ�ڷ�Ӧ��ƽ����Ӧ����v (CO2)= �������������Ӧ��CO��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ�� ��
A����߷�Ӧ�¶� B���Ƴ�����CO2 C��������ʵĴ��� D����С�������ݻ�
��4��һ���¶��µ����ܵ������ˮ��Һ�дﵽ�ܽ�ƽ��ʱ����֪�±����ݣ��Ժ������ʵ�����CuSO4��FeSO4��Fe2(SO4) 3�Ļ����Һ��˵��������ѧ����
| ���� | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25�� | 8.0��10-16 | 2.2��10-20 | 4.0��10-38 |
| ��ȫ����ʱ��PHֵ | ��9.6 | ��6.4 | 3��4 |
A. �����Һ�м��������۲��ܹ۲쵽��ɫ��������
B. ����Һ��c(SO42-)��[c(Cu2+)+c(Fe2+)+c(Fe3+)]��5:4
C. �����Һ�м���������ˮ��������pHֵ��3��4����ˣ��ɵõ�������CuSO4��Һ
D. ��û����Һ����μ���NaOH��Һ�����ȿ������ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ����Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��

�ŷ�Ӧ���� ������ȡ����ȡ�����Ӧ��
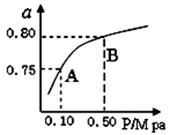
 ��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ(P)�Ĺ�ϵ����ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A) K(B)������������������������ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ����
��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ(P)�Ĺ�ϵ����ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A) K(B)������������������������ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ����
����3 L�ݻ��ɱ���ܱ������з�����Ӧ�ڣ���֪c(CO)�뷴Ӧʱ��t�仯���ߢ���ͼ��ʾ������t0ʱ�̷ֱ�ı�һ�����������ߢ��Ϊ���ߢ�����ߢ�
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��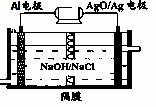
�ȼ״�ȼ�ϵ�����Ź㷺����;��ͬʱAl-AgO�����Ӧ�ù㷺������أ���ԭ����ͼ��ʾ���õ�صĸ�����Ӧʽ�� ��
��һ�������¼״���һ����̼��Ӧ���Ժϳ����ᡣͨ��״���£���a mol/L�Ĵ�����b mol/LBa(OH)2��Һ�������ϣ���Ӧƽ��ʱ��2c(Ba2��)= c(CH3COO��)���ú�a��b�Ĵ���ʽ��ʾ�û����Һ�д���ĵ��볣��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ӡˢ��·�����ɸ߷��Ӳ��Ϻ�ͭ�����϶��ɵģ�����ӡˢ��·ʱ��Ҫ��FeCl3��Ϊ����ʴҺ����ͭ����ʴ������CuCl2��FeCl2������ȫ��Ӧ��������Һ��Cu2����Fe3����Ũ��ǡ����ȡ����ѷ�Ӧ��Fe3����δ��Ӧ��Fe3�������ʵ���֮��Ϊ( )
A��1��4 B��1��2 C��2��1 D��3��1
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com