
下列对化学键的认识正确的是( )
A.化学变化中一定存在化学键的断裂和形成,物理变化中一定不存在化学键的断裂和形成
B.化学键可以使原子相结合,也可以使离子相结合
C.断裂化学键要放出能量,形成化学键要吸收能量
D.离子键、共价键、金属键、氢键均属于化学键
科目:高中化学 来源: 题型:
人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程。我们目前中学课本中的酸碱理论是1887年阿仑尼乌斯(Arrhenius)提出了的电离理论。
(1)1905年富兰克林(Franklin)把阿仑尼乌斯以水为溶剂的个别现象,推到任何溶剂,提出了酸碱溶剂理论。溶剂理论认为:凡能离解而产生溶剂正离子的物质为酸,凡能离解而产生溶剂负离子的物质为碱。试写出五氯化磷在某条件下自身电离的方程式:
▲ (一种为正四面体阳离子,另一种为正八面体阴离子)。
(2)1923年丹麦化学家布朗斯物(Brφusted)和英国化学家劳莱(Lowry)提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列粒子在水溶液既可看作酸又可看作碱的是 ▲ 。
A.HSO3- B.NH4+ C.OH- D.HCO3- E.CH3COO- F.Cl-
(3)1923年路易斯(Lewis)提出了广义的酸碱概念。凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸。如:
酸(电子对接受体) 碱(电子对给予体) 反应产物
H+ + [∶OH ]— ![]() H∶OH
H∶OH
试指出下列两个反应中的酸或碱
①H3BO3 + H2O = H+ + B(OH)4- 该反应中的碱是 ▲ (填:H3BO3 或 H2O)
②BF3 + NH3 = BF3 · NH3 该反应中的酸是 ▲ (填:BF3 或 NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:
人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程。我们目前中学课本中的酸碱理论是1887年阿仑尼乌斯(Arrhenius)提出了的电离理论。
(1)1905年富兰克林(Franklin)把阿仑尼乌斯以水为溶剂的个别现象,推到任何溶剂,提出了酸碱溶剂理论。溶剂理论认为:凡能离解而产生溶剂正离子的物质为酸,凡能离解而产生溶剂负离子的物质为碱。试写出五氯化磷在某条件下自身电离的方程式:
▲ (一种为正四面体阳离子,另一种为正八面体阴离子)。
(2)1923年丹麦化学家布朗斯物(Brφusted)和英国化学家劳莱(Lowry)提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列粒子在水溶液既可看作酸又可看作碱的是 ▲ 。
A.HSO3- B.NH4+ C.OH- D.HCO3- E.CH3COO- F.Cl-
(3)1923年路易斯(Lewis)提出了广义的酸碱概念。凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸。如:
酸(电子对接受体) 碱(电子对给予体) 反应产物
H++ [∶OH ]— H∶OH
试指出下列两个反应中的酸或碱
①H3BO3 + H2O = H+ + B(OH)4- 该反应中的碱是 ▲ (填:H3BO3 或 H2O)
②BF3 + NH3 = BF3 · NH3 该反应中的酸是 ▲ (填:BF3 或 NH3)
查看答案和解析>>
科目:高中化学 来源:2011届浙江省嵊州二中高三12月月考化学试卷 题型:填空题
人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程。我们目前中学课本中的酸碱理论是1887年阿仑尼乌斯(Arrhenius)提出了的电离理论。
(1)1905年富兰克林(Franklin)把阿仑尼乌斯以水为溶剂的个别现象,推到任何溶剂,提出了酸碱溶剂理论。溶剂理论认为:凡能离解而产生溶剂正离子的物质为酸,凡能离解而产生溶剂负离子的物质为碱。试写出五氯化磷在某条件下自身电离的方程式:
▲ (一种为正四面体阳离子,另一种为正八面体阴离子)。
(2)1923年丹麦化学家布朗斯物(Brφusted)和英国化学家劳莱(Lowry)提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列粒子在水溶液既可看作酸又可看作碱的是 ▲ 。
| A.HSO3- | B.NH4+ | C.OH- | D.HCO3- E.CH3COO- F.Cl- |
 H∶OH
H∶OH查看答案和解析>>
科目:高中化学 来源:2010-2011学年浙江省高三12月月考化学试卷 题型:填空题
人们对酸碱的认识,已有几百年的历史,经历了一个由浅入深、由低级到高级的认识过程。我们目前中学课本中的酸碱理论是1887年阿仑尼乌斯(Arrhenius)提出了的电离理论。
(1)1905年富兰克林(Franklin)把阿仑尼乌斯以水为溶剂的个别现象,推到任何溶剂,提出了酸碱溶剂理论。溶剂理论认为:凡能离解而产生溶剂正离子的物质为酸,凡能离解而产生溶剂负离子的物质为碱。试写出五氯化磷在某条件下自身电离的方程式:
▲ (一种为正四面体阳离子,另一种为正八面体阴离子)。
(2)1923年丹麦化学家布朗斯物(Brφusted)和英国化学家劳莱(Lowry)提出了质子论。凡是能够释放质子(氢离子)的任何含氢原子的分子或离子都是酸;凡是能与质子(氢离子)结合的分子或离子都是碱。按质子理论:下列粒子在水溶液既可看作酸又可看作碱的是 ▲ 。
A.HSO3- B.NH4+ C.OH- D.HCO3- E.CH3COO- F.Cl-
(3)1923年路易斯(Lewis)提出了广义的酸碱概念。凡是能给出电子对而用来形成化学键的物质是碱;凡是能和电子对结合的物质都是酸。如:
酸(电子对接受体) 碱(电子对给予体) 反应产物
H+
+ [∶OH ]—  H∶OH
H∶OH
试指出下列两个反应中的酸或碱
①H3BO3 + H2O = H+ + B(OH)4- 该反应中的碱是 ▲ (填:H3BO3 或 H2O)
②BF3 + NH3 = BF3 · NH3 该反应中的酸是 ▲ (填:BF3 或 NH3)
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
科学的发展有一个不断深化的过程。人们对有机化合物的认识同样是这样。
(1)1828年,德国化学家武勒(F?WOhler)冲破了生命力学说的束缚,在实验室里将无机物氰酸铵(NH4CNO)溶液蒸发,得到了有机物尿素[CO(NH2)2]。
|
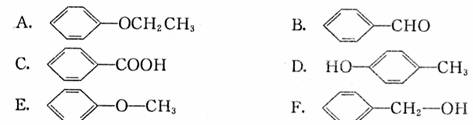
互为同分异构体的是
|
它不能解释下列 事实
(填入编号)
a.苯不能使溴水褪色
b.苯能与H2 发生加成反应
c.溴苯没有同分异构体
d.邻二溴苯只有一种
将苯与浓硫酸和硝酸混合共热并保存50℃―60℃的温度,可以生成硝基苯。反应后的仪器中有硝基苯、苯和残酸,为得到纯净的硝基苯,要进行中和、水洗,其目的是 ;已知苯的沸点是80℃,硝基苯的沸点是210.9℃,将苯与基苯分离开的实验操作是 。
(3)糖类又称碳水化合物,这是因为过去发现的糖类太多可以用通式Cn(H2O)m来表示。实际上很多符合通式为Cn(H2O)m的化合物并不属于糖类,写出两种符合通式Cn(H2O)m而不属于糖类的有机化合物的结构简式 。
(4)1830年,德国化学家李比希发展了碳、氢分析法,为有机化合物的定量分析打下了基础。某含C、H、O三种元素的未知物,经燃烧实验测定该未知物中碳的质量分数为52.16%,氢的质量分数为13.14%,则A的分子式为 。
A为有关物质存在如下转化关系,B是当今世界产量最大的塑料,广泛用于食品、医药、衣物、化肥等的包装。
![]()
写出下列反应化学方程式
①
。
② 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com