
【题目】用NaOH固体配制500mL1.0mol/L的NaOH溶液,操作步骤如下:
①把称好的NaOH固体放入小烧杯中,加适量蒸馏水溶解,冷却至室温;
②把①所得溶液小心转入容量瓶中;
③继续向容量瓶中加蒸馏水至液面距刻度线1cm~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切;
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶;
⑤将容量瓶瓶塞塞紧,充分摇匀;
⑥计算、称量NaOH固体的质量。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)⑥→①→②→___→___→⑤;
(2)所需仪器除托盘天平、药匙、烧杯、玻璃棒、胶头滴管外,还需用到的仪器有___;实验所需称量的NaOH固体为___g。
(3)试分析下列操作对所配溶液的浓度有何影响。(填“偏高”“偏低”或“无影响”)
①为加速固体溶解,可稍微加热并不断搅拌,在未降至室温时,立即将溶液转移至容量瓶定容。对所配溶液浓度的影响:___;
②定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响:___;
③定容时俯视液面。对所配溶液浓度的影响:___。
【答案】④ ③ 500mL容量瓶 20.0 偏高 偏低 偏高
【解析】
(1)根据操作过程是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶等步骤来排序;
(2)根据配制一定物质的量浓度的溶液的步骤是:计算、称量、溶解、移液、洗涤、定容、摇匀来选择使用的仪器;根据n=CV和m=nM来计算;
(3)根据c=![]() ,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差。
,通过判断不当操作对溶质的物质的量n和溶液体积V的影响来分析误差。
(1)根据操作过程是计算、称量、溶解、移液、洗涤、定容、摇匀、装瓶等步骤来排序,可知正确的操作顺序是:⑥①②④③⑤;
(2)根据配制一定物质的量浓度的溶液的步骤是计算、称量、溶解、移液、洗涤、定容、摇匀可知需要的仪器有:托盘天平、烧杯、玻璃棒、500mL容量瓶和胶头滴管,故所需的仪器还有500mL容量瓶;根据n=CV可知所需的氢氧化钠的物质的量n=1mol/L×0.5L=0.5mol,质量m=nM=0.5mol×40g/mol=20.0g;
(3)①为加速固体溶解,可稍微加热并不断搅拌.在未降至室温时,立即将溶液转移至容量瓶定容.则冷却后溶液体积偏小,所配溶液浓度偏高;
②定容后,加盖倒转摇匀后,发现液面低于刻度线是正常的,又滴加蒸馏水至刻度会导致所配溶液浓度偏低;
③定容时俯视液面,会导致溶液体积骗小,则所配溶液浓度的影响偏高。


科目:高中化学 来源: 题型:
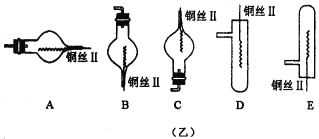
【题目】图(甲)是实验室用氢气还原氧化铜实验的微型快速实验装置.其中的粗铜丝“Ⅰ”可以在试管M中上下移动,实验前先将铜丝“Ⅰ”处理成下端弯曲的一小圆环,并用铁锤击成带小孔的小匙,虚线框中需连入图(乙)(仪器上下端位置固定)的某装置进行实验.图乙中的细铜丝“Ⅱ”一端被弯成螺旋状。
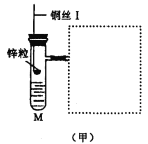
(1)在图甲中,试管M中的液体应选用_________________。
(2)在图示的虚线框中应连入的最合适的装置是___________(填代号)。
(3)上述制氢气的方法与将锌粒直接加入试管中相比,其优点有(写两点):__________________;________________ 。
(4)实验时,细铜丝“Ⅱ”的操作方法是_____________________________________________
(5)若实验室无粗铜丝,而改用无锈粗铁丝,为让其反复使用,则此时M中的液体应该是______________________,可用______________代替锌粒(写化学式), 发生反应的离子方程式为: _________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,下列溶液与1.0×10-5mol/L的NaOH溶液的pH相同的是( )
A. 把pH=6的盐酸稀释1 000倍
B. 把pH=10的Ba(OH)2溶液稀释10倍
C. 把pH=8和pH=10的NaOH溶液等体积混合
D. 把pH=8的NaOH溶液稀释10倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲用已知物质的量浓度的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视锥形瓶中颜色变化,直到加入一滴盐酸,溶液的颜色由____色变为_____,且半分钟不褪色,即停止滴定。
(2)下列操作中使所测氢氧化钠溶液的浓度数值偏高的是________(填序号)。

A、酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸
B、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后未干燥
C、酸式滴定管在滴定前有气泡,滴定后气泡消失
D、读取盐酸体积时,开始俯视读数,滴定结束时仰视读数
E、滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
(3)若滴定开始和结束时,酸式滴定管中的液面如右图所示:则起始读数为_____mL,终点读数为_____mL。
(4)如已知用c(HCl) = 0.1000 mol/L的盐酸滴定20.00 mL的氢氧化钠溶液,测得的实验数据如(3)中记录所示,则该氢氧化钠溶液的浓度c(NaOH) =____mo1/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列方程式书写正确的是 ( )
A. HCO3的电离方程式:HCO3-+H2O![]() H3O++CO32-
H3O++CO32-
B. 泡沫灭火器的原理:Al3++3HCO3- ![]() Al(OH)3↓+3CO2↑
Al(OH)3↓+3CO2↑
C. AgCl电离方程式:AgCl(s)![]() Ag+ (aq)+ Cl-(aq)
Ag+ (aq)+ Cl-(aq)
D. Na2S显碱性原因:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或应用不能用胶体的知识解释的是( )
A.土壤表面积巨大且一般带负电,能吸收NH![]() 等营养离子,使土壤具有保肥能力
等营养离子,使土壤具有保肥能力
B.清晨,人们经常看到的阳光穿过茂密的树木枝叶所产生的美丽景象
C.水泥、冶金工厂常用高压电除去工厂烟尘,减少对空气的污染
D.向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.0.1 L 1 mol/L K2SO4 溶液中含有氧原子数为0.4NA
B.67.2L氯气所含的原子数是6NA
C.常温常压下,11.2 LO2含有电子数为8NA
D.在标准状况下,2.24LN2和O2的混合气体所含原子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】pH=1的两种酸溶液HA、HB各1mL,分别加水稀释到1000mL,其pH与溶液体积(V)的关系如图所示,下列说法不正确的是
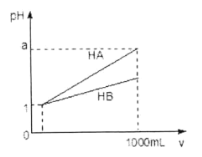
A. 同浓度、同体积的HA、HB溶液分别加入过量的锌粒,产生的氢气体积后者大
B. 物质的量浓度HA<HB
C. 若1<a<4,则HA、HB都是弱酸
D. 体积相同pH均为1的HA、HB溶液分别滴加同浓度的NaOH溶液至中性,前者消耗的NaOH少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C原子第一至第四电离能如下: I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·mol-1,I4=10540 kJ·mol-1 |
D原子核外所有p轨道全满或半满 |
E元素的主族序数与周期数的差为4 |
F是前四周期中电负性最小的元素 |
G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个方向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
![]() ,该同学所画的电子排布图违背了____________。
,该同学所画的电子排布图违背了____________。
(4)G位于第_____族_____区,该元素的核外电子排布式为_____________________________。
(5)检验F元素的方法是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com