
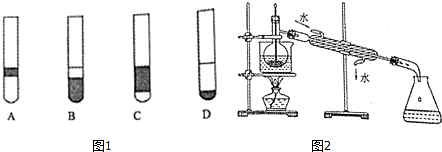
���� ��1������ɳ�Ӳ�����ˮ��ʳ������ˮ��
��2�����m=cVM���㣻
��3����ˮ�����͵Ļ����ֲ㣬��Ҫ��Һ©����Һ������CCl4��ȡ��ˮ�еĵ⣬��Ҫ��Һ©����ȡ��
��4��SiO2��NaOH��Ӧ����̼��Ʋ��ܣ�
��5���ⲻ������ˮ�����������Ȼ�̼�������Ȼ�̼���ܶȱ�ˮ���ܶȴ�
��6���Ӻ�����л���Һ��ȡ��ͻ����л��ܼ�������װ���У���ˮ�½��ϳ�����Ч���ã��¶ȼƲⶨ��ֵ��¶ȣ��Դ������
��� �⣺��1������ɳ�Ӳ�����ˮ��ʳ������ˮ������뷽��Ϊ���ˣ��ʴ�Ϊ�����ˣ�
��2������Ϊ0.5L��0.1mol/L��40g/mol=2.0g���ʴ�Ϊ��2.0��
��3����ˮ�����͵Ļ����ֲ㣬��Ҫ��Һ©����Һ������CCl4��ȡ��ˮ�еĵ⣬��Ҫ��Һ©����ȡ����ͬʹ�õ�����Ϊ��Һ©�����ʴ�Ϊ����Һ©����
��4��SiO2��NaOH��Ӧ����̼��Ʋ��ܣ����Լ�ΪNaOH��Һ�����ӷ�ӦΪSiO2+2OH-=SiO32-+H2O���ʴ�Ϊ��NaOH��Һ��SiO2+2OH-=SiO32-+H2O��
��5���ⲻ������ˮ�����������Ȼ�̼�������Ȼ�̼���ܶȱ�ˮ���ܶȴ���ֲ���²���ɫ�ֻ��D���ϣ��ʴ�Ϊ��D��
��6���Ӻ�����л���Һ��ȡ��ͻ����л��ܼ�������װ���У���ˮ�½��ϳ�����Ч���ã��¶ȼƲⶨ��ֵ��¶ȣ���ͼ��֪������Ϊ�¶ȼƲ嵽��Һ���С������ܽ���ˮ�ķ���ߵ����ʴ�Ϊ���¶ȼƲ嵽��Һ���У������ܽ���ˮ�ķ���ߵ���
���� ���⿼����������ᴿ��Ϊ��Ƶ���㣬�������ʵ����ʡ����ʲ��켰���������ᴿ����Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ʵ��װ�õ����ã���Ŀ�ѶȲ���


 ���ſ����ϵ�д�
���ſ����ϵ�д� ���Ŀ����ϵ�д�
���Ŀ����ϵ�д� ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
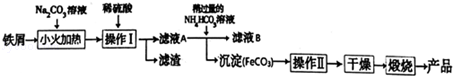
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4�� | B�� | 5�� | C�� | 6�� | D�� | 7�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=1����Һ�У�Na+��Fe3+��NO3-��I- | |
| B�� | ˮ�������c��H+��=1��10-12mol•L-1����Һ�У�K+��Al3+��Cl-��SO42- | |
| C�� | c��AlO2-��=0.1 mol•L-1����Һ�У�Na+��K+��HCO3-��Cl- | |
| D�� | ����KSCN��Һ�Ժ�ɫ����Һ��K+��NH4+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
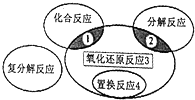 ������ԭ��Ӧ�����ֻ������ͷ�Ӧ�Ĺ�ϵ��ͼ��ʾ�������л�ѧ��Ӧ��������3���ǣ�������
������ԭ��Ӧ�����ֻ������ͷ�Ӧ�Ĺ�ϵ��ͼ��ʾ�������л�ѧ��Ӧ��������3���ǣ�������| A�� | 2H2+O2$\frac{\underline{\;��ȼ\;}}{\;}$2H2O | B�� | 2Na2HCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+CO2��+H2O | ||
| C�� | 2Na2O2+2H2O�T4NaOH+O2�� | D�� | Zn+H2SO4�TZnSO4+H2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ��Ŀ�� | ʵ�鷽�� | ��ѡ�������� | |
| A | ��ȥKNO3������NaCl | ��������Ƴ��ȵı�����Һ����ȴ�ᾧ������ | �ƾ��ơ��ձ��������� |
| B | ֤��HClO��CH3COOH������ǿ�� | ͬ������pH��ֽ�ⶨŨ��Ϊ0.1mol•L-1NaClO��Һ��0.1mol•L-1CH3COONa��Һ��pH | ������������Ƭ |
| C | ��������ˮ�������л�ԭ�� | ��������Һ�м��뼸��ϡ���ᣬˮԡ���ȼ����ӣ��������м������Ƶ�������Һ����ˮԡ���� | �Թܡ��ձ����ƾ��ơ��ι� |
| D | ����1L 1.6%��CuSO4��Һ����Һ�ܶȽ���Ϊ1g/mL�� | ��25g CuSO4•5H2O�ܽ���975ˮ�� | �ձ�����Ͳ�������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ȼ�ѧ����ʽ�У���ѧʽǰ��Ļ�ѧ������ֻ�ܱ�ʾ���ʵ��� | |
| B�� | 1 moL H2����1 mol H20ʱ�ų�����������������ȼ���ȵ�ֵ | |
| C�� | ��1mol/L�������������ϡ��Ba��OH��2��Һ��Ӧ���Բ����к��ȵ�ֵ | |
| D�� | ������ͬ����16g�������32 g������ֱ���02�г��ȼ�գ��ⶨ�����ȼ���Ȳ�ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������һ�����Ͻ� | |
| B�� | ��ά���Dz�˿����Ҫ�ɷ� | |
| C�� | ˮ���������г����Ĺ����β��� | |
| D�� | ����������������ά����Ҫԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 25�棬0.1mol/L pH=4.5 ��NaHC2O4��Һ c��HC2O4-����c��C2O42-����c��H2C2O4�� | |
| B�� | ��0.2mol/L��NaHCO3��Һ�м���������0.1mol/L��NaOH��Һc��H+��+c��Na+��=c��OH-��+c��CO32-��+c��HCO3-�� | |
| C�� | �����£��Ȼ�狀Ͱ�ˮ�Ļ����Һ��pH=7��c��Cl-��=0.1mol/L c��Cl-����c��NH4+����c��OH-��=c��H+�� | |
| D�� | Ũ�Ⱦ�Ϊ0.1mol/L�Ĵ����ƺʹ���Ļ����Һ��c��CH3COO-��-c��CH3COOH��=2[c��H+��-c��OH-��] |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com