
|
密闭容器中装有1 mol NaHCO3和0.8 mol Na2O2,加热充分反应后,容器内残留的固体是 | |
| [ ] | |
A. |
0.8 mol Na2CO3和0.6 mol NaOH |
B. |
0.5 mol Na2CO3和1 mol NaOH |
C. |
0.8 mol Na2CO3和1 mol NaOH |
D. |
1 mol Na2CO3和0.6 mol NaOH |
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源:物理教研室 题型:038
(1)如果p0小于p1,则焦炭的质量(Wg)应满足的关系是________。
(2)如果p1是p0的m倍,则W应满足的关系式是________。
查看答案和解析>>
科目:高中化学 来源: 题型:038
将一小块焦炭和ng O2同时放入一个装有压强表的密闭容器中,压强为p0;当容器内充分反应后,恢复至原温度,压强为p1。
(1)如果p0小于p1,则焦炭的质量(Wg)应满足的关系是________。
(2)如果p1是p0的m倍,则W应满足的关系式是________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省梅州市高三3月总复习质检理综化学试卷(解析版) 题型:填空题
镍具有优良的物理和化学特性,是许多领域尤其是高技术产业的重要原料。羰基法提纯粗镍涉及的两步反应依次为:
反应Ⅰ? Ni(S)+4CO(g)
 Ni(CO)4(g)△H1<0
Ni(CO)4(g)△H1<0
反应Ⅱ? Ni(CO)4(g)  Ni(S)+4CO(g) △H2??
Ni(S)+4CO(g) △H2??
(1)在温度不变的情况下,要提高反应Ⅰ中Ni(CO)4的产率,可采取的措施有???????? 、??????? 。
(2)已知350K下的2L密闭容器中装有100g粗镍(纯度98.5%,所含杂质不与CO反应),通入6 molCO气体发生反应Ⅰ制备Ni(CO)4,容器内剩余固体质量和反应时间的关系如图所示,10min后剩余固体质量不再变化。
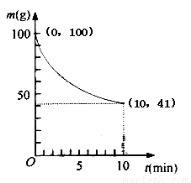
①反应Ⅰ在0~10min的平均反应速率v(Ni(CO)4)= ??????????????? 。
②若10min达到平衡时在右端得到29.5g纯镍,则反应Ⅰ的平衡常数K1为多少?(写出计算过程)
(3)反应Ⅱ中 △H2 ?? 0(填“>”、“<”、“=”);若反应Ⅱ达到平衡后,保持其他条件不变,降低温度,重新达到平衡时???????? 。(双选)
a.平衡常数K增大?? b.CO的浓度减小??? c.Ni的质量减小??? d.v逆[Ni(CO)4]增大
(4)用吸收H2后的稀土储氢合金作为电池负极材料(用MH)表示),NiO(OH)作为电池正极材料,KOH溶液作为电解质溶液,可制得高容量,长寿命的镍氢电池。电池充放电时的总反应为:
NiO(OH)+MH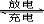 Ni(OH)2+M? 电池充电时,阳极的电极反应式为????????????????????????????????? 。电池充电时阴极上发生?????? (填“氧化”或“还原”)反应
Ni(OH)2+M? 电池充电时,阳极的电极反应式为????????????????????????????????? 。电池充电时阴极上发生?????? (填“氧化”或“还原”)反应
查看答案和解析>>
科目:高中化学 来源:河北省期末题 题型:填空题
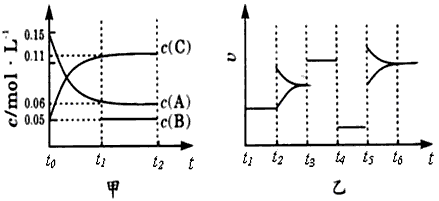
查看答案和解析>>
科目:高中化学 来源:河北省期末题 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com