
下列有关溶液中粒子浓度的关系式中正确的是( )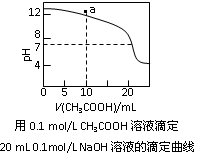
A.c(Na+)相同的①CH3COONa、②NaHCO3、③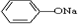 三份溶液中的pH:③>②>①
三份溶液中的pH:③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
C.上图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
D.上图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
AD
解析试题分析:因为醋酸的酸性大于碳酸,而碳酸大于苯酚,根据盐类水解的规律即越弱越水解,可以知道,c(Na+)相同的①CH3COONa、②NaHCO3、③ 三份溶液中的pH:③>②>①,故A正确;0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,根据物料守恒可以知道,c(Na+)=c(A2-)+c(HA-)+c(H2A),故B错误;图中pH=7时,c(OH-)=c(H+),因c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则c(Na+)=c(CH3COO-),故C错误;a点溶液溶质为NaOH和CH3COONa,根据电荷守恒可以得到:c(CH3COO-)+c(OH-)=c(H+)+c(Na+),根据物料守恒可以得到:c(Na+)=2c(CH3COO-)+2c(CH3COOH),二者联式可得:
三份溶液中的pH:③>②>①,故A正确;0.1mol·L-1某二元弱酸强碱盐NaHA溶液中,根据物料守恒可以知道,c(Na+)=c(A2-)+c(HA-)+c(H2A),故B错误;图中pH=7时,c(OH-)=c(H+),因c(Na+)+c(H+)=c(CH3COO-)+c(OH-),则c(Na+)=c(CH3COO-),故C错误;a点溶液溶质为NaOH和CH3COONa,根据电荷守恒可以得到:c(CH3COO-)+c(OH-)=c(H+)+c(Na+),根据物料守恒可以得到:c(Na+)=2c(CH3COO-)+2c(CH3COOH),二者联式可得:
c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH),故D正确,所以本题的答案选择AD.
考点:电离平衡,电荷守恒,物料守恒,盐类水解,离子浓度的比较
点评:本题综合考查了电离平衡,电荷守恒,物料守恒,盐类水解,离子浓度的比较,这些考点都是高考考查的重点,本题难度中等。


科目:高中化学 来源: 题型:阅读理解
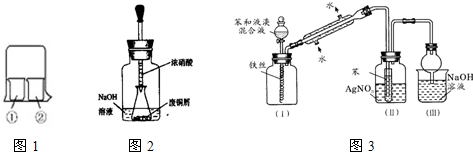
| 实验编号 | ①中的物质 | ②中的物质 |
| 1 | 淀粉碘化钾溶液 | 浓硝酸 |
| 2 | 酚酞溶液 | 浓硫酸 |
| 3 | 氯化铝溶液 | 浓氨水 |
| 4 | 湿润的红纸 | 饱和氯水 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 元素 | 有关信息 |
| X | 元素主要化合价为-2,原子半径为0.074nm |
| Y | 所在主族序数与所在周期序数之差为4 |
| Z | 原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| E | 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| ||
| ||
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
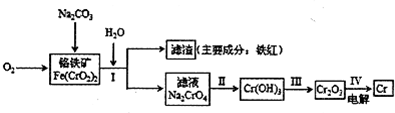
 Cr2O72-+H2O
Cr2O72-+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:

| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解




查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com