
【题目】在100℃时,将0.40 mol二氧化氮气体充入一个2 L抽空的密闭容器中,发生反应:2NO2 N2O4。每隔一段时间就对该容器内的物质进行分析,得到下表数据:
时间/s | 0 | 20 | 40 | 60 | 80 |
n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
(1)在上述条件下,从反应开始至20 s时,用NO2表示的平均反应速率为__________mol·L1·s1。
(2)n3________(填“>”“<”或“=”)n4;该反应的平衡常数K的数值为___________(精确到0.1)。
(3)若在相同条件下最初向该容器中充入N2O4,要达到上述平衡状态,N2O4的起始浓度是______mol·L1。
(4)上述(3)达到平衡后N2O4的转化率为______________,混合气体的平均摩尔质量为______________。
(5)达到平衡后,如果升高温度,气体颜色会变深,则升高温度后,反应2NO2N2O4的平衡常数将_______________(填“增大”“减小”或“不变”)。
(6)达到平衡后,如果向该密闭容器中再充入0.32 mol He,并把容器体积扩大为4 L,则平衡将______________(填“向左移动”“向右移动”或“不移动”)。
【答案】2.5×103 = 2.8 0.10 60% 57.5 g·mol1 减小 向左移动
【解析】
(1)根据方程式可知,20s时二氧化氮的变化量△n=0.05mol×2=0.1mol,根据![]() 计算二氧化氮表示的平均反应速率;
计算二氧化氮表示的平均反应速率;
(2)根据表格中数据知,60s、80s时四氧化二氮的物质的量均为0.08mol,则反应达到平衡状态;平衡时,则二氧化氮的物质的量为0.40mol-0.08mol×2=0.24mol,四氧化二氮、二氧化氮的浓度分别为0.04mol·L-1、0.12mol·L-1,进而计算平衡常数;
(3)若在相同条件下最初向该容器中充入四氧化二氮气体,要达到上述平衡状态,则该平衡状态与原平衡状态为完全等效平衡,则四氧化二氮的起始物质的量应该是0.20mol;
(4)该平衡状态与原平衡状态为完全等效平衡,平衡时,四氧化二氮的物质的量为0.08mol,二氧化氮的物质的量为0.24mol;
(5)升高温度,气体颜色会变深,说明升高温度平衡逆向移动,则平衡常数的值将减小;
(6)He是惰性气体,不参与反应,但容器体积扩大,压强减小,平衡将向气体体积减小的方向移动。
(1)根据方程式可知,20s时二氧化氮的变化量△n=0.05mol×2=0.1mol,用二氧化氮表示的平均反应速率为![]() ;
;
故答案为:2.5×103;
(2)根据表格中数据知,60s、80s时四氧化二氮的物质的量均为0.08mol,则反应达到平衡状态,则二氧化氮的物质的量也保持不变,n3=n4;平衡时,则二氧化氮的物质的量为0.40mol-0.08mol×2=0.24mol,四氧化二氮、二氧化氮的浓度分别为0.04mol·L-1、0.12mol·L-1,故平衡常数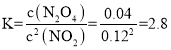 ;
;
故答案为:=;2.8;
(3)若在相同条件下最初向该容器中充入四氧化二氮气体,要达到上述平衡状态,则该平衡状态与原平衡状态为完全等效平衡,则四氧化二氮的起始物质的量应该是0.20mol,其![]() ;
;
故答案为:0.10;
(4)该平衡状态与原平衡状态为完全等效平衡,平衡时,四氧化二氮的物质的量为0.08mol,二氧化氮的物质的量为0.24mol,故转化率![]() ;混合气体的总物质的量为(0.80+0.24)mol=0.32mol,平均摩尔质量为
;混合气体的总物质的量为(0.80+0.24)mol=0.32mol,平均摩尔质量为![]() ;
;
故答案为:60%;57.5 g·mol1;
(5)升高温度,气体颜色会变深,说明升高温度平衡逆向移动,则平衡常数的值将减小;
故答案为:减小;
(6)He是惰性气体,不参与反应,但容器体积扩大,压强减小,平衡将向气体体积减小的方向移动,即向左移动;
故答案为:向左移动。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )

A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液中微粒的关系正确的是![]()
A.![]() 时,
时,![]() 的氯化铵溶液中:
的氯化铵溶液中:![]()
B.![]() 时,
时,![]() 的氯化铵溶液中:
的氯化铵溶液中:![]()
C.将![]() 的醋酸溶液稀释后,恢复至原温度,pH和
的醋酸溶液稀释后,恢复至原温度,pH和![]() 均增大
均增大
D.向![]() 溶液中加入等物质的量的NaOH形成的溶液中:
溶液中加入等物质的量的NaOH形成的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示,下列说法中正确的是![]()
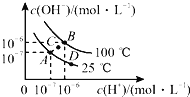
A.图中A、B、D三点处![]() 的大小关系:
的大小关系:![]()
B.若处在B点,将![]() 的硫酸与
的硫酸与![]() 的KOH溶液等体积混合,溶液显中性
的KOH溶液等体积混合,溶液显中性
C.![]() 时,保持温度不变,在水中加入适量
时,保持温度不变,在水中加入适量![]() 固体,体系可从A点变化到C点
固体,体系可从A点变化到C点
D.A点所对应的溶液中,可同时大量存在![]() 、
、![]() 、
、![]() 、
、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将H2和N2置于一容积为2 L的密闭容器中发生反应。反应过程中H2、N2和NH3的物质的量变化如图所示。
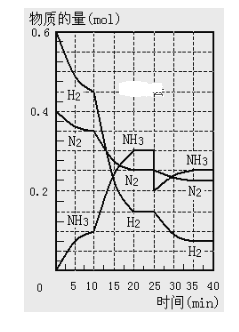
(1)反应处于平衡状态的时间段是_________________。
(2)图中10~20 min内曲线发生变化的可能原因是_______________________________________。
(3)第25 min,平衡改变的条件是____________________________________,此时正反应速率_____(填“增大”“减小”或“不变”);重新达平衡后,NH3的体积分数比原平衡______(填“大”“小”或“不变”)。
(4)判断该反应达到平衡状态的标志是___________(填字母)。
a.N2和NH3的浓度相等
b.NH3的百分含量保持不变
c.容器中气体的压强不变
d.NH3的生成速率与H2的消耗速率相等
e.容器中混合气体的密度保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元索的单质和化合物在生产生活中有重要的用途。
(1)基态溴原子的核外电子排布式为[Ar]_________。
(2)在一定浓度的HF溶液中,氟化氢是以缔合形式(HF)2存在的。使氟化氢分子缔合的作用力是_________。
(3)HIO3的酸性_________(填“强于”或“弱于”)HIO4,原因是_________。
(4)ClO2-中心氯原子的杂化类型为_________,ClO3-的空间构型为_________。
(5)晶胞有两个基本要素:①原子坐标参数:表示晶胞内部各微粒的相对位置。下图是CaF2的晶胞,其中原子坐标参数A处为(0,0,0);B处为(![]() ,
, ![]() ,0);C处为(1,1,1)。则D处微粒的坐标参数为_________。
,0);C处为(1,1,1)。则D处微粒的坐标参数为_________。


②晶胞参数:描述晶胞的大小和形状。已知CaF2晶体的密度为cg·cm-3,则晶胞中Ca2+与离它最近的F-之间的距离为_________nm(设NA为阿伏加德罗常数的值,用含C、NA的式子表示;相对原子质量:Ca 40 F 19)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg![]() 的变化如图所示,下列叙述错误的是 ( )
的变化如图所示,下列叙述错误的是 ( )

A.当lg![]() = 2时,若两溶液同时升高温度,则
= 2时,若两溶液同时升高温度,则 增大
增大
B.MOH的碱性强于ROH的碱性
C.ROH的电离程度:b点大于a点
D.两溶液分别与盐酸反应完全,则消耗HCl的物质的量相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 用饱和食盐水替代水跟电石作用,可以有效控制产生乙炔的速率
B. 食品包装材料聚乙烯因发生加成反应而易老化
C. ![]() 的名称为4—苯基—2—丁醇
的名称为4—苯基—2—丁醇
D. 重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A有如下的转化关系:
已知:![]() 当羟基与双键碳原子相连接时,易发生如下转化:
当羟基与双键碳原子相连接时,易发生如下转化:
![]()
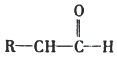
![]() 可与
可与![]() 溶液发生显色反应。
溶液发生显色反应。
![]() 的反应中,有机产物只有一种结构且能使溴水褪色。
的反应中,有机产物只有一种结构且能使溴水褪色。
请回答下列问题:
![]() 的结构简式为______。
的结构简式为______。![]() 中含有的官能团名称为______。
中含有的官能团名称为______。
![]() 的化学方程式为______,
的化学方程式为______,![]() 的化学方程式为______。
的化学方程式为______。
![]() 上述合成过程中没有涉及的反应类型有______
上述合成过程中没有涉及的反应类型有______![]() 填字母
填字母![]() 。
。
![]() 取代反应
取代反应 ![]() 酯化反应
酯化反应 ![]() 加成反应
加成反应 ![]() 消去反应
消去反应 ![]() 氧化反应
氧化反应 ![]() 还原反应
还原反应
![]() 的名称______,与F不同类且含苯环的同分异构体的结构简式为______。
的名称______,与F不同类且含苯环的同分异构体的结构简式为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com