
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-═Cl2↑ | |
| B. | NaHS水解:HS-+H2O?S2-+H3O+ | |
| C. | 在碱性介质中,氢氧燃料电池的负极反应式为:O2+4e-═2O2- | |
| D. | NaHCO3电离:NaHCO3?Na++HCO3- |
分析 A、电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电;
B、硫氢根离子水解得到的是氢硫酸和氢氧根离子;
C、氢氧燃料电池中正极上得电子发生还原反应,负极上失电子发生氧化反应;
D、碳酸氢钠是强电解质,完全电离出钠离子和碳酸氢根离子.
解答 解:A、电解饱和食盐水时,阳极上氯离子放电生成氯气,所以阳极的电极反应式为:2Cl--2e-=Cl2↑,故A正确;
B、硫氢根离子水解得到的是氢硫酸和氢离子,即HS-+H2O?H2S+OH-,故B错误;
C、氢氧燃料的正极上氧气得电子发生还原反应,正极电池反应式:O2+2H2O+4e-═4OH-,故C错误;
D、碳酸氢钠是强电解质,完全电离出钠离子和碳酸氢根离子:NaHCO3═Na++HCO3-,故D错误.
故选A.
点评 本题考查学生电极反应式、电离方程式、水解方程式的书写等知识,属于综合知识的考查,难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3溶液和NaHCO3溶液可用澄清石灰水鉴别 | |
| B. | NaHCO3比Na2CO3热稳定性强 | |
| C. | 相同质量的Na2CO3和NaHCO3与足量盐酸作用时,产生的气体质量相同 | |
| D. | 在饱和的碳酸钠溶液中通入二氧化碳溶液变浑浊 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂只有KNO3 | B. | C发生还原反应 | C. | KNO3被氧化 | D. | S得到了电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②①③④ | C. | ④①③② | D. | ③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
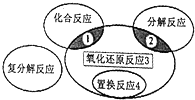 氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | 2Na2HCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | Zn+H2SO4═ZnSO4+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 绚丽缤纷的烟花中添加了含钾、钠、铁、铜等金属元素的化合物 | |
| B. | 明矾和漂白粉常用于自来水的净化,且原理相同 | |
| C. | 食用植物油的主要成分是高级脂肪酸甘油酯,是人体所需营养物质 | |
| D. | 日常生活中人们大量使用铝制品,是因为常温下铝不能与氧气反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
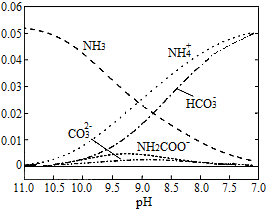 ,
,| A. | 在pH=8.0 时,c(NH4+)>c(HCO3-)>c(NH2COO-)=c(CO32-) | |
| B. | 随着C02的不断通入,Kw不变,但是水的电离受到促进 | |
| C. | 在溶液中pH不断降低的过程中,最终产物中含有NH2COO- | |
| D. | D、随着C02的通入,$\frac{c(O{H}^{-})}{c(N{H}_{3}{H}_{2}O)}$ 不断减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
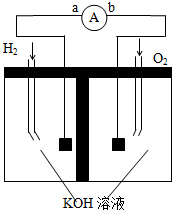 氢氧燃料电池是符合绿色化学理念的新型电池,图为电池示意图,据此回答下列问题
氢氧燃料电池是符合绿色化学理念的新型电池,图为电池示意图,据此回答下列问题查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com