
| ���� | HCOOH | HCN | H2CO3 |
| ����ƽ�ⳣ����25�棩 | K=1.77��10-4 | K=4.9��10-10 | K1=4.3��10-7��K2=5.6��10-11 |
| A�� | ��NaHCO3��Һ�У�c��OH-��-c��H+��=c��H2CO3��-c��CO32-�� | |
| B�� | ��NaCN��Һ��ͨ������CO2�����ӷ���ʽ��2CN-+H2O+CO2=2HCN+CO32- | |
| C�� | �к͵��������pH��HCOOH��HCN����NaOH����ǰ�ߴ��ں��� | |
| D�� | �����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��NaHCO3����pH��NaCN����pH��HCOONa�� |
���� ����ĵ���ƽ�ⳣ��Խ��������Խǿ����pH��������Һ������Խǿ���������ʵ���Ũ��ԽС�����������ˮ��̶�ԽС�����ǿ���ܺ������η�Ӧ��ȡ����������
��� �⣺A�����ݵ���غ㣬c��HCO3-��+c��OH-��+2c��CO32-��=c��Na+��+c��H+�����������غ�c��HCO3-��+c��H2CO3��+c��CO32-��=c��Na+�����õ���غ�-�����غ�ɵ�c��OH-��-c��H+��=c��H2CO3��-c��CO32-������A��ȷ��
B��������ǿ������˳��Ϊ��H2CO3��HCN��HCO3-������ǿ���������ԭ����֪��CN-+H2O+CO2=HCN+HCO3-����B����
C��HCOOH��HCN����һԪ�ᣬ�кͼ��������ͬ����C����
D������Խ���������ˮ��̶�Խ�����Ե����ʵ���Ũ�ȵĸ���ҺpH��ϵΪ��pH��NaCN����pH��NaHCO3����pH��HCOONa������D����
��ѡA��
���� ���⿼��������ʵĵ��룬����ƽ�ⳣ��ȷ������ǿ�����Ӷ�ȷ����֮���ת������ϵ���غ�����������Ѷ��еȣ�


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �þ���������ԭ�Ӿ��� | |
| B�� | �þ�����̼ԭ�Ӻ���ԭ�ӵĸ�����Ϊ1��2 | |
| C�� | ������̼ԭ������C-O��ѧ����֮��Ϊ1��2 | |
| D�� | ����Ŀռ���С������6��ԭ�ӹ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ��Һ��Ca2+��Ŀ���� | B�� | c��Ca2+������ | ||
| C�� | ��Һ��c��OH-������ | D�� | ��Һ��OH-��Ŀ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������105B��115B����ͬλ��ԭ�ӵ�������Ϊ1��4 | |
| B�� | 5.4 g�þ�������������Ϊ2.9 mol | |
| C�� | �������ķֱ���105B��115B���ɵľ���������������֮��Ϊ6��5 | |
| D�� | ��̼ԭ������Ϊw g����105Bԭ�ӵ�����Ϊ10w g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
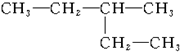 3-������
3-������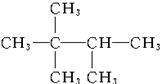 2��2��3-��������
2��2��3-��������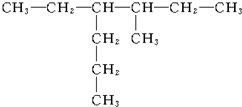 3-��-4-�һ�����
3-��-4-�һ�����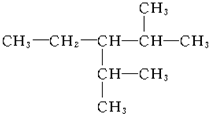 2��5-����-3-�һ�����
2��5-����-3-�һ�����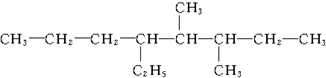 3��4-����-5-�һ�����
3��4-����-5-�һ�����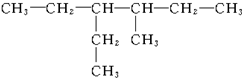 3-��-4-�һ����飮
3-��-4-�һ����飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��1 | B�� | 5��4 | C�� | 4��3 | D�� | 5��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com