
可逆反应A(aq)+B(aq) C(l)+D(aq) ΔH=-50kJ·mol-1,下列有关该反应的叙述正确的是
C(l)+D(aq) ΔH=-50kJ·mol-1,下列有关该反应的叙述正确的是
A.正反应活化能小于50 kJ·mol-1
kJ·mol-1
B.逆反应活化能不小于50 kJ·mol-1
C.正反应活化能大于50 kJ·mol-1
D.逆反应活化能比正反应活化能小50 kJ·mol-1
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2016-2017学年湖北省高二12月月考化学试卷(解析版) 题型:实验题
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL。
试回答下列问题:
(1)锥形瓶中的溶液从 色变为 色时,停止滴定。
(2)滴定时边滴边摇动锥形瓶,眼睛应观察 。
A、滴定管内液面的变化 B、锥形瓶内溶液颜色的变化
(3)该小组在步骤①中的 错误是 由此造成的测定结果 (偏高、偏低或无影响)
错误是 由此造成的测定结果 (偏高、偏低或无影响)
(4)步骤②缺少的操作是 。
(5)如图,是某次滴定时的滴定管中的液面,其读数为 mL

(6)请计算待测烧碱溶液的浓度 mol/L。
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前度数(mL) | 滴定后度数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨中学高二上期末化学试卷(解析版) 题型:选择题
下列实验中,对应的现象以及解释或结论都正确且具有因果关系的是:
选项 | 操作 | 现象 | 解释或结论 |
A | 测定等浓度的Na2CO3和Na2SO3溶液的pH | Na2CO3溶液的pH较大 | 非金属性C<S |
B | 向盛有2ml 0.1mol/L AgNO3溶液的试管中滴加一定量0.1mol/L NaCl溶液,再向其中滴加一定量 0.1mol/L KI溶液 | 先有白色沉淀生成,后又 | Ksp(AgCl)> Ksp(AgI) |
C | 室温下,取相同大小、形状和质量的Cu粒分别投入0.1m | Cu粒与浓硝酸反应比与稀硝酸反应剧烈 | 探究浓度对化学反应速率的影响 |
D | 用石墨做电极电解Mg(NO3)2、Cu(NO3)2的混合溶液 | 阴极上先析出铜 | 金属活动性:Mg>Cu |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年西藏拉萨北京实验中学高二上期末化学卷(解析版) 题型:选择题
用标准盐酸滴定未知浓度的NaOH溶液,下列操作不会引起实验误差的是 ( )
A.用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定
C.用碱式滴定管取10.00 mL NaOH溶液放入锥形瓶中,加入少量的蒸馏水再进行滴定
D.用酚酞作指示剂滴至红色刚变无色时即停止加盐酸
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二12月月考化学卷(解析版) 题型:选择题
NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将浓度均为0.020 mol·L-1NaHSO3(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如右图。据图分析,下列判断不正确的是
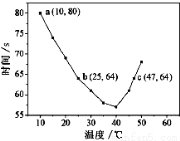
A .40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中b、c两点对应的NaHSO3反应速率不等
C.图中a点对应的NaHSO3反应速率为5.0 ×10-5mol·L-1·s-1
D.温度高于40℃时,淀粉适宜用作该试验的指示剂
查看答案和解析>>
科目:高中化学 来源:2016-2017年陕西西藏民族学院附中高二12月月考化学卷(解析版) 题型:填空题
常温下,将0.01molNH4Cl和0.005molNaOH溶于水配成1L溶液(pH>7).
(1)该溶液中存在的三个平衡体系是 、 、 。
(2)溶液中存在的离子物质的量浓度由大到小顺序为 。
(3)这些粒子中浓度为0.01mol/L的是 ,浓度为0.005mol/L的是 。
(4)物质的量之和为0.0lmol的二种粒子是 。
(5)NH4+和H+两种粒子物质的量之和比OH-多 mol。
查看答案和解析>>
科目:高中化学 来源:2016-2017年陕西西藏民族学院附中高二12月月考化学卷(解析版) 题型:选择题
在298 K、101kPa时,己知:
2H2O(g)=2H2(g) +O2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2
2Cl2(g) +2H2O(g)=4HCl(g)+O2(g) △H3
则△H3与△H1和△H2间的关系正确的是
A.△H3= △H1+2△H2 B.△H3=△H1 +△H2
C.△H3= △H1- 2△H2 D.△H3=△H1-△H2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西西安一中高二上月考二化学卷(解析版) 题型:选择题
为了除去MgCl2溶液中的FeCl3,可在加热搅拌的条件下加入一种试剂,该试剂是
A.NaOH B.Na2CO3 C.氨水 D.MgO
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上月考四化学卷(解析版) 题型:选择题
化学电池可以直接将化学能转化为电能,化学电池的本质是
A.化合价的升降
B.电子的转移
C.氧化还原反应
D.电能的储存
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com