
(1)哪些是金属元素?__________。
(2)D与A的简单离子是 __________。
(3)__________元素的氢氧化物碱性最强。
(4)B与D的两原子间能形成的化合物是____________________(写出化学式)。?
科目:高中化学 来源: 题型:
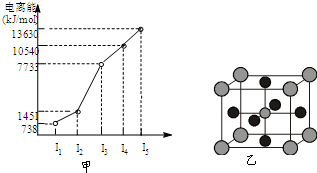 有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.
有X、Y、Z、W四种元素,原子序数依次减小.已知X是第四周期的主族元素,其部分电离能如图甲所示;X、Y元素具有相同的最高正化合价;Z 原子p轨道共有3个电子;W原子价电子排布式为nsnnpn.查看答案和解析>>
科目:高中化学 来源: 题型:
有第四周期的A、B、C、D四种元素,其价电子数依次为1、2、2、7,其原子序数依A、B、C、D依次增大。已知A与B的次外层电子数为8,而C与D为18。根据原子结构,判断:
(1)哪些是金属元素?__________。
(2)D与A的简单离子是 __________。
(3)__________元素的氢氧化物碱性最强。
(4)B与D的两原子间能形成的化合物是____________________(写出化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源:期中题 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com