
某同学进行如下实验,探究化学反应中的能量变化。
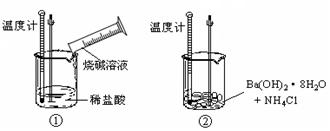
通过实验测出,反应前后①烧杯中的温度升高,②烧杯中的温度降低。由此判断NaOH溶液跟盐酸的反应是 (填 “吸热”或“放热”)反应,Ba(OH)2· 8H2O跟NH4Cl的反应是 (填“吸热”或“放热”)反应。反应①中反应物的总能量 填(“大于”、“小于”或“等于”)生成物的总能量。反应②中断开反应物中的化学键所吸收的能量 填(“大于”、“小于”或“等于”)形成生成物中的化学键所放出的能量。
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)化学式为C8Hm的烷烃,m值等于
(1)化学式为C8Hm的烷烃,m值等于查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2SO3已部分被空气中的氧气氧化 | B、加入Ba(NO3)2溶液后,生产的沉淀中一定含有BaSO4 | C、加硝酸后的不溶性沉淀是BaSO3和BaSO4 | D、此实验不能确定Na2SO3是否被部分氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com