
【题目】下列有关反应热的叙述正确的是
A.已知![]()
![]()
![]() ,则氢气的燃烧热为
,则氢气的燃烧热为![]()
B.![]() ,石墨
,石墨![]() ,金刚石
,金刚石![]() ,说明石墨比金刚石稳定
,说明石墨比金刚石稳定
C.![]() ,
,![]() 恒温恒容条件下达到平衡后加入X,上述反应的
恒温恒容条件下达到平衡后加入X,上述反应的![]() 增大
增大
D.已知![]() ;
;![]() 则
则![]()
科目:高中化学 来源: 题型:
【题目】已知一定温度下合成氨反应:N2(g)+3H2(g)2NH3(g) ΔH=-92.4kJmol-1,在恒温恒压的密闭容器中进行如下实验:①通入1molN2和3molH2,达平衡时放出热量为Q1,②通入2molN2和6molH2,达平衡时放出热量为Q2,则下列关系正确的是( )
A.2Q1<Q2B.Q2=184.8kJ
C.Q1<Q2=184.8kJD.Q2=2Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W,其中X、Z、W与氢元素可组成共价化合物XH3、H2Z和HW;Y与氧元素可形成离子化合物Y2O和Y2O2。
(1)Y2Z的电子式是 ________
(2)实验室可用如图所示装置制备并收集XH3(缺少收集装置,夹持固定装置略去)。

①图中方框内应选用连接_____烧瓶收集XH3(填“A或B”)。
②实验室制法中大试管中的试剂一般选用(填写化学式)_________________。烧杯中溶液由无色变为红色,其原因是(用电离方程式表示):___________________________________
③XH3是工业上氧化法制硝酸的重要基础原料,制备过程中该物质发生的化学反应方程式为__________________________。
(3)磷在W2中燃烧可生成两种产物,其中一种产物甲,分子中各原子最外层不全是8电子结构,甲的化学式是_________。 XH3和HW两种化合物能反应生成离子化合物乙,n mol甲与n mol乙在一定条件下反应,生成4n mol HW和另一化合物,该化合物蒸气的密度是相同状况下氢气密度的174倍,其化学式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤、石油是人类目前使用的主要能源,同时也是重要的化工原料。
Ⅰ.石油经分馏、裂化、裂解可以获得C4H10、CH4、C3H6、C2H6、C2H4等许多重要的化工原料。
已知:i.C4H10(g)![]() CH4(g)+C3H6(g)
CH4(g)+C3H6(g)
ii.C4H10(g)![]() C2H6(g)+C2H4(g)
C2H6(g)+C2H4(g)
CH3CH2CH2CH3与![]() 的平衡转化率随温度变化的关系如图1所示。
的平衡转化率随温度变化的关系如图1所示。

(1)![]() 的名称是___;其一氯代物有___种,结构简式分别是___。
的名称是___;其一氯代物有___种,结构简式分别是___。
(2)660℃时,取1molCH3CH2CH2CH3通入2L恒容密闭容器中发生反应i、ii,经过30min达到平衡,C2H6的体积分数为![]() 。
。
①达平衡时反应物转化率为___,30min内,用C2H6表示的平均反应速率v(C2H6)为___。
②达到平衡时,CH4的物质的量分数为___%(精确到0.1)。
Ⅱ.用煤干馏得到的二甲苯和乙烯为原料合成涤纶(聚酯纤维)的路线如下:

(3)①写出A![]() B的化学方程式:__,反应类型是___。
B的化学方程式:__,反应类型是___。
②若1mol![]() 与1mol
与1mol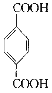 酯化反应的生成物中含两个环,写出该物质的结构简式:___;若生成物中只含一个环,写出反应的化学方程式___。
酯化反应的生成物中含两个环,写出该物质的结构简式:___;若生成物中只含一个环,写出反应的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮气是制备含氮化合物的一种重要物质,而含氮化合物的用途广泛。图中表示两个常见的固氮反应:
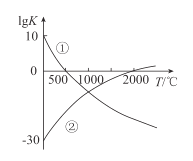
①![]()
②![]() 的平衡常数
的平衡常数![]() 与温度的关系,根据图中的数据判断下列说法正确的是( )
与温度的关系,根据图中的数据判断下列说法正确的是( )
A.反应②为放热反应
B.常温下,反应①的反应速率很大,而反应②的反应速率很小
C.升高温度,反应①的反应速率增大,反应②的反应速率减小
D.在常温下,利用反应①固氮和利用反应②固氮反应程度相差很大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于说法正确的是( )
A. HCl和NaOH反应的中和热△H=﹣57.3 kJ/mol。则H2SO4和Ba(OH)2反应的中和热△H=2×(﹣57.3) kJ/mol
B. 已知C2H5OH(l)的燃烧热是1366.8 kJ/mol,则C2H5OH(l)+3O2(g) ═ 2CO2(g)+3H2O(g) 反应的△H=-1366.8 kJ/mol
C. 一定条件下2SO2(g)+O2(g)![]() 2SO3(g) △H1<0,2SO2(g)+O2(g)
2SO3(g) △H1<0,2SO2(g)+O2(g)![]() 2SO3(l) △H2<0,则△H1>△H2
2SO3(l) △H2<0,则△H1>△H2
D. 在一定温度和压强下,将0.5mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放出热量19.3 kJ,则其热化学方程式为N2(g)+3H2(g)![]() 2NH3(g) △H=﹣38.6kJ/mol
2NH3(g) △H=﹣38.6kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写热化学方程式:
(1)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应的中和热的热化学方程式______________________________;
(2)25℃、101 kPa条件下充分燃烧一定量的丁烷气体放出热量为QkJ,经测定,将生成的CO2通入足量澄清石灰水中产生25 g白色沉淀,写出表示丁烷燃烧热的热化学方程式_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚( CH3OCH3)。请回答下列问题:
(1)利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g)![]() CH3OH(g) △H= -90.8kJ/mol
CH3OH(g) △H= -90.8kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-41.3kJ/mol
CO2(g)+H2(g) △H=-41.3kJ/mol
总反应:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g) 的△H= ;
CH3OCH3(g)+CO2(g) 的△H= ;
一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是:________(填字母代号)。
a.压缩体积 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度e.分离出二甲醚(CH3OCH3)
(2)已知反应②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-23.5kJ/mol
某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
物质 | CH3OH | CH3OCH3 | H2O |
浓度(mol·L-1) | 0.40 | 0.6 | 0.6 |
①比较此时正、逆反应速率的大小比较:![]() _________
_________![]() (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②该反应的平衡常数的表达式为K=_____,温度升高,该反应的平衡常数K____(填“增大”、“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向2 L恒容密闭容器中加入2 mol X、1 mol Y。发生如下反应:2X(g)+Y(?)![]() 3Z(g) ΔH=-a kJ·mol-1(a>0)。经60 s达平衡,此时Y的物质的量为0.2 mol。下列说法错误的是( )
3Z(g) ΔH=-a kJ·mol-1(a>0)。经60 s达平衡,此时Y的物质的量为0.2 mol。下列说法错误的是( )
A.0~60 s内,用Z表示的化学反应速率为1.2 mol·L-1·min-1
B.若再充入1 mol Z,重新达到平衡时,X的体积分数不变,则Y为气态
C.达平衡后,实际放出的热量为b kJ,则b=a
D.若Y为气态,则使容器体积变为1 L,Z的物质的量不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com