
| A. | ①②③④ | B. | ②⑤⑥⑦ | C. | ①③④⑤⑥ | D. | 除①②外 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 除去Fe粉中混有的I2:加热使I2升华 | |
| B. | 除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶 | |
| C. | 除去碳酸钠中混有的碳酸氢钠:加入过量的氢氧化钠溶液,蒸发结晶 | |
| D. | 除去氯气中含有的氯化氢气体:用饱和食盐水洗涤后干燥 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在氧化还原反应中,甲比乙失电子多 | |
| B. | 同价态的阳离子,甲比乙氧化性强 | |
| C. | 甲能与稀硫酸反应生成氢气而乙不能 | |
| D. | 甲的最高价氧化物的水化物的碱性弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
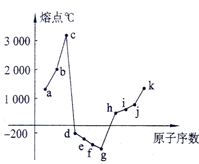 在1-18号元素中,部分连号元素单质的熔点情况如图所示,试回答:
在1-18号元素中,部分连号元素单质的熔点情况如图所示,试回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①③ | B. | 只有②③④ | C. | 只有①③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 向水中加入NaOH溶液,平衡逆向移动,c(OH-)降低 | |
| B. | 向水中加入少量固体NaHSO4,c(H+)增大,Kw不变 | |
| C. | 向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低? | |
| D. | 将水加热,Kw增大,pH变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 一定温度下在体积为5L的密闭容器中发生可逆反应.
一定温度下在体积为5L的密闭容器中发生可逆反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6和C4H10一定是同系物 | |
| B. | C2H4和C4H8一定是同系物 | |
| C. | C3H6不只表示一种物质 | |
| D. | 烯烃中各同系物中碳的质量分数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 负极反应Al-3e-Al3+ | B. | 燃料气体是氧气 | ||
| C. | 正极反应为2CO2+O2+4e-2CO32- | D. | 该电池不能用烃类物质作燃料 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com