
| A�� | ����MnCO3��Ŀ���dz�ȥFe3+ | |
| B�� | �����£�pH=4ʱ��Fe3+�ѳ��� | |
| C�� | ��ӦCu2+��aq��+MnS��s��=CuS��s��+Mn2+��aq����K=1.35��1022 | |
| D�� | Mn2��OH��2CO3��Mn��OH��2���������MnCO3 |
���� �ɸ����ʵ�Ksp��С��֪��������Һ��pH��������Fe��OH��3����������Ksp��CuS��Ksp��MnS������ʹMnSת����CuS�����ȥ��������Һ�к���CuSO4��Fe2��SO4��3���ʣ�����Һ�м���MnCO3��Ҳ�ɼ���Mn2��OH��2CO3��Mn��OH��2��������ҺpH������Fe��OH��3��������ַ�Ӧ���ˣ��ټ���MnS��������CuS���Դ˽����⣮
��� �⣺A����Ksp[Fe��OH��3]=4.0��10-38����֪Fe��OH��3�����ɳ������ɼ���MnCO3��������ҺpH�����ã��ɳ�ȥFe3+����A��ȷ��
B��Ksp[Fe��OH��3]=4.0��10-38����Fe3+�ѳ���ʱ��c��OH-��=$\root{3}{\frac{4.0��1{0}^{-38}}{1��1{0}^{-5}}}$mol/L=1.58��10-11mol/L��pH��3.7����B��ȷ��
C����ӦCu2+��aq��+MnS��s��=CuS��s��+Mn2+��aq����K=$\frac{c��M{n}^{2+}��}{c��C{u}^{2+}��}$=$\frac{Ksp��MnS��}{Ksp��CuS��}$=$\frac{4.65��1{0}^{-14}}{6.3��1{0}^{-36}}$=0.74��1022����C����
D��Mn2��OH��2CO3��Mn��OH��2��MnCO3�������ƣ������������ӷ�Ӧ���ɶ�����̼��ˮ�������������ʣ��ɴ��棬��D��ȷ��
��ѡC��
���� ���⿼�����ܵ���ʵ��ܽ�ƽ�⣬Ϊ�߿��������ͺ�Ƶ���㣬������ѧ���ķ��������ͼ��������Ŀ��飬ע������ܶȻ������弰Ӧ�ã�������ؼ��㷽�����Ѷ��еȣ�


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 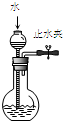 ͼ1��ʾװ�ÿɼ��װ�������� | |
| B�� | 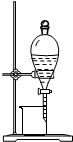 ͼ2��ʾװ�ÿɴӵ��CCl4��Һ�з������ | |
| C�� | 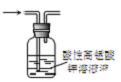 ͼ3��ʾװ�ÿɳ�ȥ��������ϩ | |
| D�� | 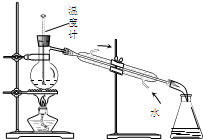 ͼ4��ʾװ�ÿɷ���ױ����Ҵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
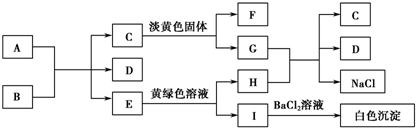
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 ��R��R�����������
��R��R�����������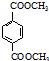 �ж���ͬ���칹�壬ͬʱ��������������ͬ���칹����8�֣�
�ж���ͬ���칹�壬ͬʱ��������������ͬ���칹����8�֣� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �� | |||||||||||||||||
| �� | �� | �� | �� | ||||||||||||||
| �� | �� | �� | |||||||||||||||
| �� | �� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������ձ������ʯ���� | |
| B�� | ��ȥ�Ҵ��е����ᣬ����NaOH��Һ���Һ | |
| C�� | ����0.1mol•L-1NaCl��Һ��ʵ���У���������ƽ��ȡ5.85gNaCl | |
| D�� | ������ͭ��Һ����Ũ������ȴ�ᾧ�õ�CuSO4•5H2O���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
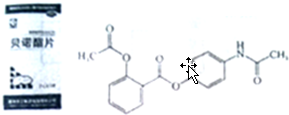
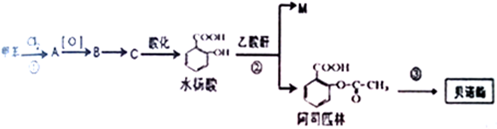
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���ᷴӦ 2Fe+6H+�T2Fe3++3H2�� | |
| B�� | ����������Һ�еμ��Ȼ�����Һ Ba2++SO42-�TBaSO4�� | |
| C�� | ��ˮ���뵽�廯����Һ�� Br-+Cl2�TBr2+Cl- | |
| D�� | ̼�������ϡ���� CO32-+2H+�TH2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 �˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ�������Fe2O3��TiO2������������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ��
�˹��̵���ָ����Ԫ��������̬ת��Ϊ����̬�Ĺ��̣��ݱ��������¡���ѹ�����������£�N2�ڲ�������Fe2O3��TiO2������������ˮ������Ӧ�����ɵ���Ҫ����ΪNH3����Ӧ���Ȼ�ѧ����ʽΪ���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com