


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.200 | 0.100 | 0.080 | 0.050 | 0.050 | 0.050 |
| n(O2)(mol) | 0.100 | 0.050 | 0.040 | 0.025 | 0.025 | 0.025 |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省济宁市高三第一次模拟理综化学试卷(解析版) 题型:填空题
2013年12月15日4时搭载长征系列火箭的“玉兔号”顺利驶抵月球表面,实现了五星红旗耀月球的创举。火箭升空需要高能燃料,通常用肼(N2H4)作燃料,N2O4做氧化剂。请回答下列问题:
(1)已知:N2(g) + 2O2(g) == 2NO2(g)????????????????? ΔH= + 67.7kJ·mol-1
N2H4(g) + O2(g)== N2(g) + 2H2O(g)????? ΔH= - 534.0kJ·mol-1
2NO2(g)  N2O4(g)????????????? ΔH= - 52.7kJ·mol-1
N2O4(g)????????????? ΔH= - 52.7kJ·mol-1
写出气态肼在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:?????????????????????????????????? ;
(2)工业上用次氯酸钠与过量的氨气反应制备肼,该反应的化学方程式为:???????????????????????????????????? ;
(3)工业上可以用下列反应原理制备氨气:
2N2(g)+6H2O(l) 4NH3(g)+3O2(g)?? ΔH= Q kJ·mol-1
4NH3(g)+3O2(g)?? ΔH= Q kJ·mol-1
①已知该反应的平衡常数K与温度的关系如图,则此反应的 Q ?????? 0 (填“>”“<”或“=”)。
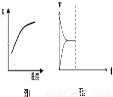
②若起始加入氮气和水,15分钟后,反应达到平衡,此时NH3的浓度为0.3mol/L,则用氧气表示的反应速率为??????????? 。
③常温下,如果上述反应在体积不变的密闭容器中发生,当反应达到平衡时, ???????? (选填编号).
A.容器中气体的平均相对分子质量不随时间而变化????
B.v(N2)/v(O2)=2∶3
C.容器中气体的密度不随时间而变化
D.通入稀有气体能提高反应的速率
E.若向容器中继续加入N2,N2的转化率将增大
(4)最近华南理工大提出利用电解法制H2O2并以此处理废氨水,装置如图。
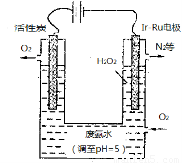
①为不影响H2O2的产量,需要向废氨水加入适量硝酸调节溶液的pH约为5,则所得废氨水溶液中c(NH4+) ?????? c(NO3-)(填“>”“<”或“=”);
②Ir—Ru惰性电极有吸附O2作用,该电极的电极反应为????????????????????? ;
③理论上电路中每转移3mol电子,最多可以处理NH3·H2O的物质的量为???????????? 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年云南省毕业生复习统一检测理综化学试卷(解析版) 题型:填空题
2013年12月2日,我国在西昌卫星发射中心用“长征三号甲”运载火箭将“嫦娥三号”探月卫星成功送入太空,进一步向广寒宫探索。“长征三号甲”是三级液体助推火箭,一、二级为常规燃料,常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。
Ⅰ.常规燃料通常指以肼(N2H4)为燃料,以二氧化氮做氧化剂。但有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大(两者反应生成氮气和氟化氢气体)。
已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H = -543kJ·mol-1
 H2(g)+
H2(g)+  F2(g)
= HF(g) △H = -269kJ·mol-1
F2(g)
= HF(g) △H = -269kJ·mol-1
H2(g)+  O2(g)
= H2O(g) △H = -242kJ·mol-1
O2(g)
= H2O(g) △H = -242kJ·mol-1
请写出肼和氟气反应的热化学方程式:_____________________________。
Ⅱ.氧化剂二氧化氮可由NO和 O2生成,已知在2 L密闭容器内,800 ℃时反应:
2NO(g)+O2(g) 2NO2(g)
ΔH 的体系中,n(NO)随时间的变化如表:
2NO2(g)
ΔH 的体系中,n(NO)随时间的变化如表:
|
时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
|
n(NO)(mol) |
0.200 |
0.100 |
0.080 |
0.050 |
0.050 |
0.050 |
|
n(O2)(mol) |
0.100 |
0.050 |
0.040 |
0.025 |
0.025 |
0.025 |
(1) 已知:K800℃>K1000℃,则该反应的ΔH ______0(填“大于”或“小于”),用O2表示从0~2 s内该反应的平均速率为__________。
(2)能说明该反应已达到平衡状态的是________。
a.容器内颜色保持不变 b. 2v逆(NO)=v正(O2)
c.容器内压强保持不变 d.容器内密度保持不变
(3)为使该反应的速率增大,提高NO的转化率,且平衡向正反应方向移动应采取的措施有 。
(4)在上述条件下,计算通入2 mol NO和1 mol O2的平衡常数K=______________。
(5)在上述条件下,若开始通入的是0.2 mol NO2气体,达到化学平衡时,则NO2的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
人民网西昌报道组2013年12月2日01时30分,玉兔号宣布成功发射。据早些时候报道,昨天上午9时起,工作人员开始为“玉兔号”和长三丙火箭加注常规燃料,至14时30分左右加注的是燃烧剂;此后至18时左右加注氧化剂。

甲:玉兔号发射瞬间 乙:运行中的玉兔号
已知A、B、C、D是元素周期表中的四种短周期元素,且原子序数依次增大,A的单质是上述资料中的“燃烧剂”,C的单质是上述资料中的“氧化剂”;A元素原子中没有中子;bB与cC两种元素存在关系:b = c﹣1;C元素常见化合价的绝对值与其所在周期数相同,且B、C能形成多种气态化合物,其中一种可以在大自然状态下形成;A、D两种元素形成的双原子分子的水溶液是工业三大强酸之一。
请解答下列问题:
(1)A元素在元素周期表第 族中,D元素在元素周期表第 周期中。
(2)B原子的原子结构示意图: 。
(3)A、B两种元素形成的四原子分子的电子式为 。
(4)上图甲中发生反应的化学方程式为: 。
(5)A、B形成的六原子分子BA2—BA2也可以作为火箭发射中的燃烧剂,此时往往使用
C形成的四原子分子(A2C2)作为氧化剂。已知8g 液态BA2—BA2与足量液态A2C2反应,生成均为无害气体,放出热量为160.35kJ。
请写出上述反应的热化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com