B
分析:A、常温常压下,气体摩尔体积大于22.4L/mol.
B、O
2、O
3都是由氧元素组成,48g为氧原子质量,根据n=

计算氧原子物质的量,再根据N=nN
A计算氧原子数目.
C、物质的量相同的N
2和CO所含分子数目相同,但二者的物质的量不一定是1mol.
D、0.9%NaCl溶液是指氯化钠质量分数,不是物质的量浓度.溶液密度不知道,无法计算钠离子数目.
解答:A、压强一定,气体摩尔体积受温度影响,温度越高气体摩尔体积越大,常温常压下,气体摩尔体积大于22.4L/mol
,22.4LCO
2的物质的量小于1mol,含有CO
2分子数小于N
A个,故A错误;
B、O
2、O
3都是由氧元素组成,48g为氧原子质量,氧原子物质的量为
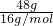
=3mol,含有的氧原子数目为3mol×N
Amol
-1=3N
A,故B正确;
C、物质的量相同的N
2和CO所含分子数目相同,但二者的物质的量不一定是1mol,所含分子数目不一定是N
A,故C错误;
D、0.9%NaCl溶液是指氯化钠质量分数,不是物质的量浓度.溶液密度不知道,无法计算钠离子数目,故D错误.
故选:B.
点评:考查常用化学计量的有关计算与理解,难度不大,注意通过PV=nRT理解气体摩尔体积及气体摩尔体积使用条件与对象.

 计算氧原子物质的量,再根据N=nNA计算氧原子数目.
计算氧原子物质的量,再根据N=nNA计算氧原子数目.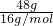 =3mol,含有的氧原子数目为3mol×NAmol-1=3NA,故B正确;
=3mol,含有的氧原子数目为3mol×NAmol-1=3NA,故B正确;

 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案