
科目:高中化学 来源:2016-2017学年重庆市高二上第一次月考化学卷(解析版) 题型:选择题
下列有关实验的说法正确的是
A. 用湿润的pH试纸测稀盐酸的pH
B. 用酸式滴定管量取20.00 mL酸性K2Cr2O7溶液
C. 用托盘天平称取5.85 gNaCl晶钵
D. 用带磨口玻璃塞的试剂瓶保存Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| A | 基态原子的价电子排布式为nSnnPn |
| B | 基态原子中的未成对电子数是同周期中最多的 |
| C | 最外层电子数是电子层数的3倍 |
| D | 简单离子是第三周期元素中离子半径最小的 |
| E | 价电子层中的未成对电子数为4 |
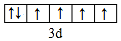 .
.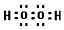 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )
如图所示,将两烧杯中电极用导线相连,四个电极分别为Mg、Al、Pt、C.当闭合开关S后,以下表述正确的是( )| A. | 电流表指针不发生偏转 | |
| B. | Al、Pt两极有H2产生 | |
| C. | 甲池pH增大,乙池pH减小 | |
| D. | Mg、C两极生成的气体在一定条件下可以恰好完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 水溶液中能电离出H+的化合物叫做酸 | |
| B. | 实验测得2mol某气体体积为44.8L,则测定条件一定是标准状况 | |
| C. | 摩尔是七个基本物理量之一 | |
| D. | 化合物分为酸、碱、盐和氧化物是用树状分类法分类的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
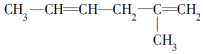 被酸性高锰酸钾氧化的产物的是( )
被酸性高锰酸钾氧化的产物的是( )| A. | CO2 | B. | CH3COOH | ||
| C. | 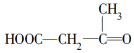 | D. | HOOC-CH2-CH2-COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
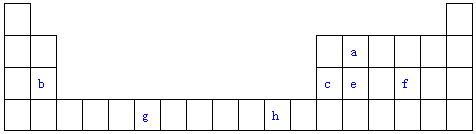
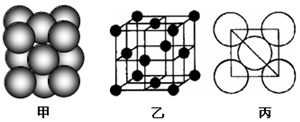
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 催化液化I中使用催化剂,反应的活化能Ea、△H2都减小 | |
| B. | 反应C(s)+H2O(g)+H2(g)=CH3OH(g)△H=41.1 kJ•mol-1 | |
| C. | △H2>△H3 | |
| D. | 图为甲醇燃料电池的工作原理,负极的电极反应为:CH3OH-6e-+6OH-═CO2+5H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com