
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)具有良好的热稳定性、耐热性、电绝缘性,是目前用量最大的热稳定剂,工业上利用铅废渣(主要含PbSO4、 PbCl2、 SiO2)制取三盐基硫酸铅及PbO2工艺流程如下:

已知:①“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2+SO42-(aq)和
PbCl2+SO42-(aq)和
PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,
PbCl42-(aq) △H>0,
②Ksp(PbCl2)=1.7×10-5 Ksp(PbSO4)=2.5×10-8
回答下列问题:
(1)铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和___________。
(2)“操作1”通过多步操作得到PbCl2,分别为___________、___________、过滤、洗涤。
(3)“转化”后得到PbSO4,当c(Cl-)=0.100mol/L时,c(SO42-)=___________(结果保留一位小数);“转化”时需要升高体系温度,其原因是_________________________________。
(4)写出合成三盐基硫酸铅的化学方程式_________________________________。
(5)氨水络合后铅的存在形态是[ Pb(OH)SO4]-,写出“氧化”发生的离子反应方程式__________________________________________________________________。
(6)一种新型的铅锂电池的充放电示意图如下,写出放电时的正极反应式___________。

【答案】SiO2 蒸发浓缩 冷却结晶 1.5×10-5mol/L 升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)![]() PbSO4(s)+2HCl(aq)向右移动 4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O [Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O Li1-xMn2O4+xe-+xLi+=LiMn2O4
PbSO4(s)+2HCl(aq)向右移动 4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O [Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O Li1-xMn2O4+xe-+xLi+=LiMn2O4
【解析】
铅废渣(主要含PbSO4、 PbCl2、 SiO2)加入CaCl2 、NaCl溶液,“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2+SO42-(aq)和PbCl2(s)+2Cl-(aq)
PbCl2+SO42-(aq)和PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2,“操作1”通过多步操作得到PbCl2,分别为蒸发浓缩、冷却结晶、过滤、洗涤。加入硫酸“转化”后得到PbSO4,溶液Ⅱ为HCl,加入NaOH合成三盐基硫酸铅,反应为:4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O,加NH3·H2O络合后溶解生成[ Pb(OH)SO4]-,加入(NH4)2S2O82-发生[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O,得PbO2。
PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2,“操作1”通过多步操作得到PbCl2,分别为蒸发浓缩、冷却结晶、过滤、洗涤。加入硫酸“转化”后得到PbSO4,溶液Ⅱ为HCl,加入NaOH合成三盐基硫酸铅,反应为:4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O,加NH3·H2O络合后溶解生成[ Pb(OH)SO4]-,加入(NH4)2S2O82-发生[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O,得PbO2。
(1)铅废渣(主要含PbSO4、 PbCl2、 SiO2)加入CaCl2 、NaCl溶液,“浸出”过程发生的反应:PbSO4(s)+2Cl-(aq)![]() PbCl2(s)+SO42-(aq)和PbCl2(s)+2Cl-(aq)
PbCl2(s)+SO42-(aq)和PbCl2(s)+2Cl-(aq)![]() PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2;
PbCl42-(aq) △H>0,铅渣“浸出”后,“浸出渣”的主要成分是CaSO4和SiO2;
(2)“操作1”分别经过蒸发浓缩、冷却结晶、过滤、洗涤得到PbCl2晶体。
(3)“转化”后得到PbSO4,PbSO4(s)+2Cl-(aq)![]() PbCl2(s)+SO42-(aq),当c(Cl-)=0.100mol/L时,c(SO42-)=c2(Cl-)Ksp(PbSO4)/Ksp(PbCl2)=0.1002×2.5×10-8/1.7×10-5=1.5×10-5;“转化”时需要升高体系温度,其原因是升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)
PbCl2(s)+SO42-(aq),当c(Cl-)=0.100mol/L时,c(SO42-)=c2(Cl-)Ksp(PbSO4)/Ksp(PbCl2)=0.1002×2.5×10-8/1.7×10-5=1.5×10-5;“转化”时需要升高体系温度,其原因是升高温度有利于HCl逸出,使PbCl2(s)+H2SO4(aq)![]() PbSO4(s)+2HCl(aq)向右移动。
PbSO4(s)+2HCl(aq)向右移动。
(4)已知三盐基硫酸铅(3PbO·PbSO4·H2O),反应物为PbSO4和NaOH,合成三盐基硫酸铅的化学方程式4PbSO4+6NaOH=3PbO·PbSO4·H2O+3Na2SO4+2H2O。
(5)3PbO·PbSO4·H2O氨水络合后铅的存在形态是[ Pb(OH)SO4/span>]-,+2价铅氧化成+4价,“氧化”发生的离子反应方程式[Pb(OH)SO4]-+S2O82-+3OH-=PbO2↓+3SO42-+2H2O。
(6)新型的铅锂电池放电时正极发生还原反应,正极反应式Li1-xMn2O4+xe-+xLi+=LiMn2O4。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】CO2是主要的温室气体,也是一种工业原料。回收利用CO2有利于缓解温室效应带来的环境问题。
(1)我国科学家通过采用一种新型复合催化剂,成功实现了CO2直接加氢制取高辛烷值汽油。
已知:2H2 (g)+O2 (g) =2H2O(l) ΔH = -571.6 kJ/mol
2C8H18(l)+25O2(g) =16CO2(g)+18H2O(l) ΔH = -11036 kJ/mol

25℃、101kPa条件下,CO2与H2反应生成辛烷(以C8H18表示)和液态水的热化学方程式是_________。
(2)CO2催化加氢合成乙醇的反应原理是:2CO2(g)+6H2(g)![]() C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=
C2H5OH(g)+3H2O(g) △H =-173.6 kJ/mol图是起始投料不同时,CO2的平衡转化率随温度的变化关系,m为起始时的投料比,即m=![]() 。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
。m1、m2、m3投料比从大到小的顺序为_________,理由是_________。
(3)在Cu/ZnO催化剂存在下,将CO2与H2混合可合成甲醇,同时发生以下两个平行反应:
反应Ⅰ CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
CH3OH(g)+H2O(g) ΔH1=-53.7 kJ/mol
反应Ⅱ CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
控制一定的CO2和H2初始投料比,在相同压强下,经过相同反应时间测得如下实验数据(其中“甲醇选择性”是指转化的CO2中生成甲醇的百分比):
实验序号 | T/K | 催化剂 | CO2转化率/% | 甲醇选择性/% |
实验1 | 543 | Cu/ZnO纳米棒 | 12.3 | 42.3 |
实验2 | 543 | Cu/ZnO纳米片 | 10.9 | 72.7 |
实验3 | 553 | Cu/ZnO纳米棒 | 15.3 | 39.1 |
实验4 | 553 | Cu/ZnO纳米片 | 12.0 | 71.6 |
①对比实验1和实验3可发现:同样催化剂条件下,温度升高,CO2转化率升高, 而甲醇的选择性却降低,请解释甲醇选择性降低的可能原因_______________;
②对比实验1和实验 2可发现:在同样温度下,采用Cu/ZnO纳米片使CO2转化率降低, 而甲醇的选择性却提高,请解释甲醇的选择性提高的可能原因____________。
③有利于提高CO2转化为CH3OH平衡转化率的措施有_______。
a.使用Cu/ZnO纳米棒做催化剂
b.使用Cu/ZnO纳米片做催化剂
c.降低反应温度
d.投料比不变,增加反应物的浓度
e.增大![]() 的初始投料比
的初始投料比
(4)以纳米二氧化钛膜为工作电极,稀硫酸为电解质溶液,在一定条件下通入CO2,电解,在阴极可制得低密度聚乙烯![]() (简称LDPE)。
(简称LDPE)。
①电解时,阴极的电极反应式是_____________。
②工业上生产1.4×104 kg 的LDPE,理论上需要标准状况下______L 的CO2。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g)![]() N2O4(g);ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如下图。下列说法中,正确的是
N2O4(g);ΔH<0。现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如下图。下列说法中,正确的是

A.反应速率:v正(b点)<v正(d点)
B.前10min内用v(N2O4)表示的平均反应速率为0.04mol/(L·min)
C.25min时,导致平衡移动的原因是升高温度
D.a和c点:Qc(浓度熵)<K(平衡常数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列现象或操作涉及改变蛋白质的生理活性的是( )
①打针用医用酒精对皮肤消毒
②用稀的甲醛溶液浸泡作物种子消毒
③用硫酸铜制成的农药波尔多液防治农作物病虫害
A.仅①②B.仅③C.仅①③D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】港珠澳大桥水泥的使用量约198万吨。水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙含量的过程如图所示:
下列叙述正确的是

A. 水泥、玻璃、陶瓷为传统的硅酸盐材料,三者的原料都主要为SiO2
B. 沉淀A主要成分为SiO2,沉淀B为Fe(OH)3、Al(OH)3
C. 为了加快溶解速率,使用盐酸代替硫酸处理草酸钙
D. 草酸钙易溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,电池反应为:4Li+FeS2=Fe+2Li2S。下列说法不正确的是

A. 该装置将化学能转化为电能
B. 可以用水代替 SO(CH3)2做溶剂
C. 电子移动方向是由a极经外电路流向b极
D. b极电极反应式是:FeS2+4Li++4e-=Fe+2Li2S
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。反应A:![]()
已知:i. 反应A中,4mol HCl被氧化,放出115.6kJ的热量。
ii.
![]()
①HCl的电子式是__________。
②反应A的热化学方程式是____________。
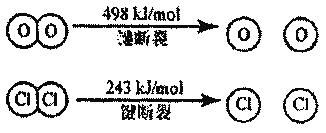
③断开1mol H-O键与断开1mol H-Cl键所需能量相差约______kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)_____。
(2)下图是容积均为1L,分别按4种投料比[n(HCl):n(O2)]分别为1:1、2:1、4:1、6:1进行投料,反应温度对HCl平衡转化率影响的曲线。
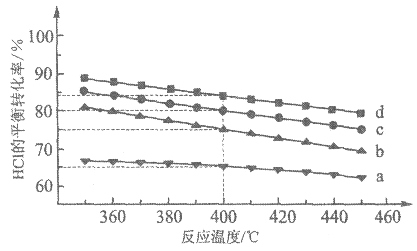
①曲线c对应的投料比是__________。
②用平衡移动的原理解释温度和HCl平衡转化率的关系__________。
③投料比为4:1、温度为400℃时,平衡混合气中Cl2的物质的量分数是_____,O2的平衡转化率______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com