
【题目】Ⅰ、有机物分子中的一个碳原子所连的4个原子或原子团均不相同时,该碳原子称为手性碳原子,含有手性碳原子的化合物具有光学活性,某有机物X(结构如下)具有光学活性(式中标有*号的碳为手性碳原子),欲使其保持光学活性,发生以下 (选填序号)反应,该有机物仍一定具有光学活性。
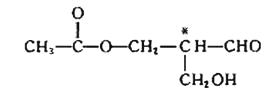
A.消去反应 | B.水解反应 | C.银镜反应 | D.酯化反应 |
Ⅱ、写出由1-溴丁烷和必要的无机试剂制取1,2-二溴丁烷的化学方程式
【答案】Ⅰ、C
Ⅱ、CH2BrCH2CH2CH3+NaOH![]() CH2=CHCH2CH3↑+NaBr+H2O;
CH2=CHCH2CH3↑+NaBr+H2O;
CH2=CHCH2CH3+Br2→CH2BrCHBrCH2CH3
【解析】试题分析:Ⅰ、根据X的结构简式可知,A.发生消去反应后*号碳原子形成碳碳双键,只能连接3个原子或原子团,不再具有光学活性;B.发生水解反应后*号碳原子连接两个相同的-CH2OH,不再具有光学活性;C.发生银镜反应后,-CHO变成-COOH,产物中*号碳原子仍然连接4个不相同的原子或原子团,具有光学活性;D.如果与醋酸发生酯化反应,产物不具有光学活性;若与其他酸酯化,则产物具有光学活性,故D不符合题意。
故答案为:C。
Ⅱ、1-溴丁烷和必要的无机试剂制取1,2-二溴丁烷分为两个步骤,化学方程式可表示为:CH2BrCH2CH2CH3+NaOH![]() CH2=CHCH2CH3↑+NaBr+H2O;CH2=CHCH2CH3+Br2→CH2BrCHBrCH2CH3。
CH2=CHCH2CH3↑+NaBr+H2O;CH2=CHCH2CH3+Br2→CH2BrCHBrCH2CH3。
故答案为:CH2BrCH2CH2CH3+NaOH![]() CH2=CHCH2CH3↑+NaBr+H2O;CH2=CHCH2CH3+Br2→CH2BrCHBrCH2CH3。
CH2=CHCH2CH3↑+NaBr+H2O;CH2=CHCH2CH3+Br2→CH2BrCHBrCH2CH3。


科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物
(1)工业上尿素由CO2和NH3合成,写出其方程式 ___________________________.
(2)当氨碳比![]() 时,CO2的转化率随时间的变化关系如图所示。
时,CO2的转化率随时间的变化关系如图所示。

①A点的逆反应速率v逆(CO2)________B点的正反应速率v正(CO2)(填“大于”“小于”或“等于”)。
②NH3的平衡转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学--选修5:有机化学基础]氰基丙烯酸酯在碱性条件下能快速聚合为![]() ,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
,从而具有胶黏性,某种氰基丙烯酸酯(G)的合成路线如下:
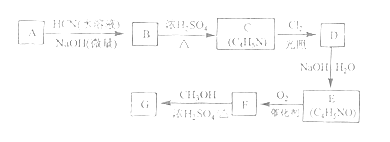
已知:①A的相对分子量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A的化学名称为_______。
(2)B的结构简式为______,其核磁共振氢谱显示为______组峰,峰面积比为______。
(3)由C生成D的反应类型为________。
(4)由D生成E的化学方程式为___________。
(5)G中的官能团有_____、 _____ 、_____。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有_____种。(不含立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
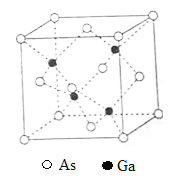
【题目】[化学——选修3:物质结构与性质]砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。回答下列问题:
(1)写出基态As原子的核外电子排布式________________________。
(2)根据元素周期律,原子半径Ga_____________As,第一电离能Ga____________As。(填“大于”或“小于”)
(3)AsCl3分子的立体构型为____________________,其中As的杂化轨道类型为_________。
(4)GaF3的熔点高于1000℃,GaCl3的熔点为77.9℃,其原因是_____________________。
(5)GaAs的熔点为1238℃,密度为ρg·cm-3,其晶胞结构如图所示。该晶体的类型为________________,Ga与As以________键键合。Ga和As的摩尔质量分别为MGa g·mol-1和MAs g·mol-1,原子半径分别为rGa pm和rAs pm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
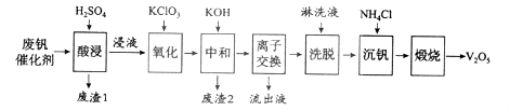
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
R4V4O12+4OH(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”、“碱”或“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利科学家使用普通氧分子和带正电的氧离子作用,制出了新型的氧分子O4,它的结构很复杂,可能具有与S4相似的长方形结构,是一种高能量分子。
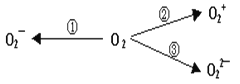
(1)下列有关O4的说法正确的是:
A.O4分子内存在极性共价键
B.合成O4的反应可看作核聚变反应,不属于化学变化
C.O4与O3、O2都是氧的同素异形体
D.O4将来可用作更强有力的火箭推进的氧化剂
(2)制备含O2-、O22-甚至O2+的化合物都是可能的,通常它们是在氧分子进行下列各种反应时生成的:上述变化中, (填序号)相当于氧分子被氧化; _______(填序号)相当于氧分子被还原。
(3)写出O22—的电子式: (4) O2+、O2-中的电子数分别为: ; __。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(普通)化合物H是重要的有机物,可由E和F在一定条件下合成:(部分反应物或产物省略,另请注意箭头的指向方向)
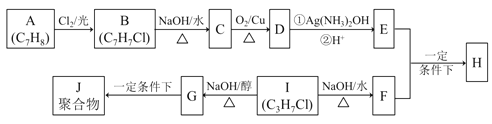
已知以下信息:
i.A属于芳香烃,H属于酯类化合物。
ii.I的核磁共振氢谱为二组峰,且峰的面积比为6:1。
回答下列问题:
(1)E的含氧官能团名称 ,B的结构简式 。
(2)B → C和G → J两步的反应类型 , 。
(3)① E + F → H的化学方程式 。
② I → G 的化学方程式 。
(4)I的同系物K比I相对分子质量大28,K有多种同分异构体。
①K的同分异构体共 种。
②若K不能发生消去反应,则K的结构简式为_________ _。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法不正确的是
A.蔗糖水解生成互为同分异构体的葡萄糖和果糖
B.用灼烧的方法可以区分蚕丝和人造纤维
C.C4H9Cl有4种同分异构体
D.油脂和蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(1)该反应的离子方程式为 。
(2)用“双线桥”表示出反应中电子转移的方向和数目:
KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O
(3)氧化产物与还原产物的质量之比为 。
(4)如果反应中转移0.2mol电子,则生成I2的物质的量为_________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com