
有关电化学知识的描述正确的是( )
A.CaO+H2O===Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能
B.某原电池反应为Cu+2AgNO3===Cu(NO3)2+2Ag,装置中的盐桥中可以是装有含琼胶的KCl饱和溶液
C.原电池的两极一定是由活动性不同的两种金属组成
D.从理论上讲,任何能自发进行的氧化还原反应都可设计成原电池
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
按要求填空(均为短周期元素)
(1)最外层电子数为1的元素有______(填元素符号,下同)。
(2)最外层电子数为2的元素有______。
(3)最外层电子数与次外层电子数相等的元素有______。
(4)最外层电子数是次外层电子数2倍的元素是______。
(5)最外层电子数是次外层电子数3倍的元素是______。
(6)次外层电子数是最外层电子数2倍的元素有______。
(7)内层电子总数是最外层电子数2倍的元素有______。
(8)电子层数与最外层电子数相等的元素有______。
(9)最外层电子数是电子层数2倍的元素有______。
(10)最外层电子数是电子层数3倍的元素有______。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学研究性学习小组的同学在学习了氨气的性质后讨论:既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题。请你参与该小组的活动并完成下列实验:
Ⅰ.制取氨气
(1)实验室常用加热氯化铵固体和氢氧化钙固体混合物的方法来制取氨气。写出实验室制取氨气的化学方程式:______________________________________________________。
(2)实验室还可向____________(填一种试剂)中滴加浓氨水的方法快速制取少量氨气。
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气。你认为能否达到目的?________(填“能”或“否”),理由是___________________。
Ⅱ.实验探究
该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出)探究氨气的还原性(生成Cu和无污染的物质):

(1)写出氨气与CuO反应的化学方程式:___________________________________。
(2)为达到上述实验目的,预期的实验现象①________________________;②________________________________________________________________________。
(3)该装置在设计上有一定的缺陷,为确保实验结果的准确性,对该装置的改进措施是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2是一种大气污染物,某兴趣小组欲探究SO2的性质及绿色实验方法,设计如下方案:
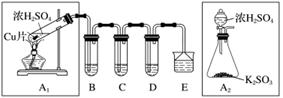
(1)B、C、D分别用于检验SO2的漂白性、还原性和氧化性。其中C、D分别为碘水和硫化氢的水溶液,则B中所盛试剂为__________,C中反应的离子方程式为________________________________________________________________________。
(2)为了实现绿色实验的目标,某同学重新设计了如上右图A2的制取装置来代替A1装置,与A1装置相比,A2装置的优点是____________________________________________________
(任写一点即可)。
(3)E中用氨水吸收尾气中的SO2,“吸收液”中可能含有OH-、SO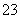 、SO
、SO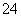 、HSO
、HSO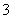 等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol·L-1盐酸、2 mol·L-1 HNO3、1 mol·L-1 BaCl2溶液、1 mol·L-1 Ba(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO
等阴离子。已知亚硫酸氢盐一般易溶于水,SO2也易溶于水。现有仪器和试剂为小烧杯、试管、玻璃棒、胶头滴管、过滤装置和滤纸;2 mol·L-1盐酸、2 mol·L-1 HNO3、1 mol·L-1 BaCl2溶液、1 mol·L-1 Ba(OH)2溶液、品红溶液、蒸馏水。请设计实验证明“吸收液”中存在SO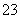 和HSO
和HSO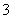 ,完成下表的实验操作、预期现象和结论:
,完成下表的实验操作、预期现象和结论:
| 实验操作 | 预期现象与结论 |
| 步骤1:取适量“吸收液”于小烧杯中,用胶头滴管取1 mol·L-1 BaCl2溶液滴入小烧杯中直至过量 | 若出现白色浑浊,则溶液中存在SO |
| 步骤2:将小烧杯中的浊液过滤、洗涤,再用适量水把附在滤纸上的固体冲入另一小烧杯中;向冲下的固体______________ | |
| 步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4SOCl2。电池的总反应可表示为4Li+2SOCl2===4LiCl+S+SO2↑。
请回答下列问题:
(1)电池的负极材料为__________,发生的电极反应为
________________________________________________________________________。
(2)电池正极发生的电极反应为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:锂离子电池的总反应为LixC+Li1-xCoO2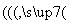 C+LiCoO2
C+LiCoO2
锂硫电池的总反应为2Li+S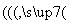 Li2S
Li2S
有关上述两种电池说法正确的是( )
A.锂离子电池放电时,Li+向负极迁移
B.锂硫电池充电时,锂电极发生还原反应
C.理论上两种电池的比能量相同
D.下图表示用锂离子电池给锂硫电池充电
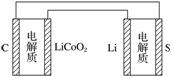
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25 ℃时,FeS、CuS的溶度积常数(Ksp)分别为6.3×10-18、1.3×10-36。常温时下列有关说法正确的是( )
A.除去工业废水中的Cu2+可以选用FeS作沉淀剂
B.将足量CuSO4溶解在0.1 mol·L-1 H2S溶液中,Cu2+的最大浓度为1.3×10-35 mol·L-1
C.因为H2SO4是强酸,所以反应CuSO4+H2S===CuS↓+H2SO4不能发生
D.向H2S的饱和溶液中通入少量SO2气体,溶液的酸性增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com