
【题目】某物质A在一定条件下加热完全分解,产物都是气体。分解方程式为 4A=B+2C+2D,测得生成的混合气体对氢气的相对密度为2 d,则A的相对分子质量为( )
A. 7d B. 5d C. 2.5d D. 2d
科目:高中化学 来源: 题型:
【题目】下列有关说法错误的是( )
A. 硅可用于制造光导纤维 B. 氧化铁可作涂料和红色油漆
C. 铝热反应可用于焊接铁轨 D. 呈液态的钠钾合金可用于原子反应堆的热交换剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3晶体是一种常见的氧化剂,生产工艺如图所示:
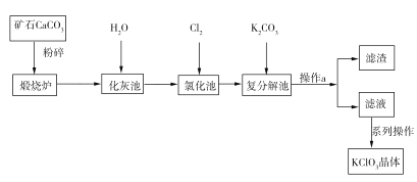
请回答下列问题:
(1)CaCO3煅烧前要粉碎的目的是____________________________。
(2)写出“氯化池”中生成Ca(ClO3)2的化学方程式:___________________________。该反应中,氧化剂与还原剂的物质的量之比为________。
(3)操作a中所需的玻璃仪器有漏斗、烧杯、__________。
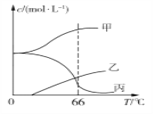
(4)实验室制取KClO3可通过反应:3Cl2+6KOH![]() 5KCl+KClO3+3H2O,在密闭容器中向9 ℃的KOH溶液中通入少量Cl2,此时Cl2的氧化产物主要是________________;继续通入适量Cl2,将溶液加热,溶液中主要离子的浓度随温度的变化如图所示,图中甲、乙、丙依次表示的离子是_________。(不考虑Cl2的挥发)
5KCl+KClO3+3H2O,在密闭容器中向9 ℃的KOH溶液中通入少量Cl2,此时Cl2的氧化产物主要是________________;继续通入适量Cl2,将溶液加热,溶液中主要离子的浓度随温度的变化如图所示,图中甲、乙、丙依次表示的离子是_________。(不考虑Cl2的挥发)
(5)甲同学为测定制取的KClO3样品中ClO3的含量,称取样品a g,准确配制成1000 mL溶液,从上述溶液中取出10.00 mL于锥形瓶中,准确加入30.00 mL 1.00 mol·L1 (NH4)2Fe(SO4)2溶液(过量)。再在锥形瓶中加入100 mL蒸馏水及某种氧化还原反应指示剂,用0.200 mol·L1 K2Cr2O7标准溶液滴定至终点,消耗5.00 mL。样品中ClO3的质量分数为______________。(已知:Cr2O72-+6Fe2++14H+![]() 2Cr3++6Fe3++7H2O,ClO3可被Fe2+还原为Cl。)
2Cr3++6Fe3++7H2O,ClO3可被Fe2+还原为Cl。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g) ![]() 2N2+3H2O(g) ΔH<0,在恒容的密闭容器中,下列有关说法正确的是 ( )
2N2+3H2O(g) ΔH<0,在恒容的密闭容器中,下列有关说法正确的是 ( )
A. 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大
B. 平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小
C. 单位时间内消耗NO和N2的物质的量比为1∶2时,反应达到平衡
D. 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染:
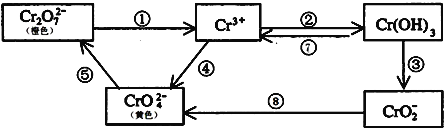
完成下列填空:
(1)含Cr2O72-离子的废水在酸性条件下用Fe3O4处理,反应的离子方程式如下,配平该离子反应方程式:
_____Cr2O72-+Fe3O4+H+→Cr3++Fe3++H2O
(2)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应:阳极_____________________ 阴极_______________________;用铁做阳极的目的是:_____________________
(3)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:______________________
(4)已知Ag2CrO4和AgCl的Ksp分别为9.0×10-12、1.56×10-10,向含有相同浓度的Na2CrO4和NaCl的混合溶液中逐滴加入硝酸银溶液,首先生成的沉淀是__________
(5)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:① Cr2O72- +6I- + 14H+ →3I2 + 2Cr3+ + 7H2O ② 2S2O32- + I2→S4O62- + 2I- ,准确称取纯净的K2Cr2O7 0.294g ,配成溶液,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。则Na2S2O3溶液的物质的量浓度为_____________________(保留四位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关。下列叙述中不正确的是
A.将少量二氧化硫添加到红酒中可起到杀菌和抗氧化作用
B.将电器垃圾深埋处理可减少重金属对环境的危害
C.对化学燃料脱硫、脱氮可减少酸雨的形成
D.用CO2合成聚碳酸酯可降解塑料可实现碳的循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固态化合物A由两种短周期元素组成,可与水发生复分解反应,甲组同学用下图装置(夹持装置略)对其进行探究实验。
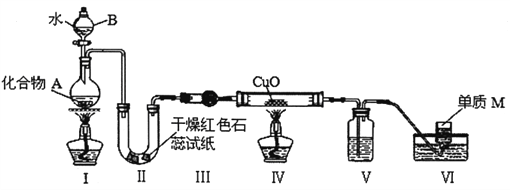
(1)仪器A的名称是________,仪器B在该实验中有两个作用:一是控制反应速度,二是_______________________。
(2)试验中,II中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成。
①Ⅲ中的试剂为________________;
②Ⅳ发生反应的化学方程式为_____________________________;
③V的作用为_______________;装置V的缺陷是___________________.
(3)乙组同学进行同样实验,但装置连接顺序为I-Ⅲ一Ⅳ- II-V-Ⅵ,此时II中现象为__________,
原因是_______________________。
(4)化合物A中含单质M的元素的质量分数为28%,则A的化学式为____________,写出A与水反应的化学方程式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一Na2SO3、Na2SO4混合物样品ag,为了测定其中Na2SO3的质量分数,设计了如下方案,其中明显不合理的是( )
A.将样品配制成溶液V1L,取其中25.00mL恰好与V2mL浓度为cmol/L酸性KMnO4溶液完全反应
B.向样品中加足量H2O2 , 再加足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为bg
C.将样品与足量稀盐酸充分反应后,再加入足量BaCl2溶液,过滤,将沉淀洗涤、干燥,称量其质量为c g
D.将样品与足量稀盐酸充分反应,生成的气体依次通过盛有饱和NaHSO3的洗气瓶、盛有浓H2SO4的洗气瓶、盛有碱石灰的干燥管Ⅰ、盛有碱石灰的干燥管Ⅱ,测定干燥管Ⅰ增重d g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作使所配溶液的浓度偏小的是
A. 定容摇匀后发现溶液凹面低于刻度线,加水至刻度线
B. 用量筒量取浓盐酸时,仰视刻度线
C. 定容时,俯视刻度线
D. 容量瓶在使用前未干燥,里面有少量蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com