
| A. | 127I与131I互为同素异形体 | B. | 137Cs的核电荷数为137 | ||
| C. | 铀235的中子数是143 | D. | 铯与水的反应比钠与水的反应缓慢 |
分析 A.由同种元素形成的不同种单质互为同素异形体;
B.元素符号的左下角为核电荷数;
C.中子数=质量数-质子数;
D.同一主族,从上倒下,元素的金属性逐渐增强,与水反应越剧烈.
解答 解:A.同素异形体是单质,而131I和127I都是原子,所以131I和127I不互为同素异形体,二者互为同位素,故A错误;
B.137Cs的核电荷数为55,故B错误;
C.中子数=质量数-质子数=235-92=143,故C正确;
D.铯(Cs)与钠同主族,铯(Cs)与水的反应比钠与水的反应剧烈,故D错误.
故选C.
点评 本题考查质量数、质子数以及中子数之间的关系以及元素周期律等,比较基础,侧重对基础知识的巩固,注意对基础知识的理解掌握.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| a | |||||||
| b | c | d | |||||
| e | f | g |
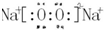 ;b、g元素形成的bg2作为溶剂可溶解S单质(填写该单质“名称”或“化学式”)
;b、g元素形成的bg2作为溶剂可溶解S单质(填写该单质“名称”或“化学式”)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸滴在银片上:2Ag+2H+═2Ag++H2↑ | |
| B. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-═BaSO4↓ | |
| C. | 硝酸银溶液与盐酸反应:Ag++Cl-═AgCl↓ | |
| D. | 澄清石灰水与碳酸钠溶液反应:Ca(OH)2+CO32-═CaCO3↓+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
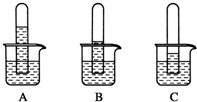
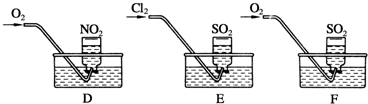
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
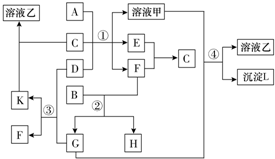
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向水中投入一小块金属钠 | B. | 将水加热煮沸 | ||
| C. | 向水中通入二氧化碳气体 | D. | 向水中加醋酸钠晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑥⑦ | B. | ①⑤⑦ | C. | ②③④ | D. | ②④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com