

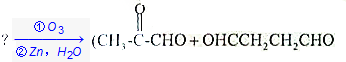

 ��
�� +��m-1��H2O����B-C��C-E�ķ�Ӧ���ͷֱ�Ϊ���ӳɷ�Ӧ�����۷�Ӧ��
+��m-1��H2O����B-C��C-E�ķ�Ӧ���ͷֱ�Ϊ���ӳɷ�Ӧ�����۷�Ӧ�� ���� ��1��������Ϣ̼̼˫����������Ӧ������п�۴�����ˮ�⣬���ѳ����˵�̼ԭ�Ӹ����һ����ԭ�Ӷ���ȩ����ͪ�������Ѻ��CH2���ɼ�ȩ��CH-CH�ṹ�����Ҷ�ȩ��C��CH3��2�ṹ���ɱ�ͪ��
��2����1mol��2mol Br2��ȫ�ӳɣ������������2��˫����1��������C7H10��������Ӧ������п�۴�����ˮ�����ɣ��������ȩ����λ��Ϊ̼̼˫��������λ�ã�
��3���߷��ӻ����C4H5Cl��n��������Ӧ������п�۴�����ˮ�⣬˵��A�к���̼̼˫����B�ܷ���������Ӧ˵������ȩ����B�������ӳ����ɺ��д��ǻ���C��C��Ũ����������·���������Ӧ������Ԫ������˵��C�л��������ᣬ�������������ӳɣ�˵��B�к������ᣬ������Ϣ����������Ȼ��ϵ��Ȼ���±Ԫ��ԭ��ȡ����������サ��±����±����һˮ��Ӧ�����Ը߷��ӻ����C4H5Cl��nΪ ����������Ӧ������п�۴�����ˮ�⣬BΪOHCCH2CH2COOH����������Ӧ����CΪHOCH2CH2COOH��C��������������Ӧ������EΪ��
����������Ӧ������п�۴�����ˮ�⣬BΪOHCCH2CH2COOH����������Ӧ����CΪHOCH2CH2COOH��C��������������Ӧ������EΪ�� ��C�������۷�Ӧ������D
��C�������۷�Ӧ������D ���ݴ˷������
���ݴ˷������
��� �⣺��1��������Ϣ̼̼˫����������Ӧ������п�۴�����ˮ�⣬���ѳ����˵�̼ԭ�Ӹ����һ����ԭ�Ӷ���ȩ����ͪ������ӦΪ��CH2=CH-CH=C��CH3��2$��_{��Zn��H_{2}O}^{��O_{3}}$HCHO+OHCCHO+CH3COCH3��
�ʴ�Ϊ��CH2=CH-CH=C��CH3��2$��_{��Zn��H_{2}O}^{��O_{3}}$HCHO+OHCCHO+CH3COCH3��
��2��C7H10��������Ӧ������п�۴�����ˮ������CH3COCHO��OHCCH2CH2CHO���������ȩ����λ��Ϊ̼̼˫��������λ�ã�C7H10��1mol��2mol Br2��ȫ�ӳɣ������������2��˫����7��̼�ı�����ΪC7H16������C7H10Ϊ��������2��˫����������ṹ��ʽΪ�� ��
��
�ʴ�Ϊ�� ��
��
��3���߷��ӻ����C4H5Cl��n��������Ӧ������п�۴�����ˮ�⣬˵��A�к���̼̼˫����B�ܷ���������Ӧ˵������ȩ����A��B����C4H5Cl��n$��_{��Zn��H_{2}O}^{��O_{3}}$OHCCH2CH2COOH+HCl��
B�������ӳ����ɺ��д��ǻ���C��C��Ũ����������·���������Ӧ������Ԫ������˵��C�л��������ᣬ�������������ӳɣ�˵��B�к������ᣬB��C��OHCCH2CH2COOH+H2$\stackrel{����}{��}$HOCH2CH2COOH��
C��Ũ����������·���������Ӧ������Ԫ������C��E��HOCH2CH2COOH$��_{��}^{Ũ����}$ +H2O��C�������۷�Ӧ��m HOCH2CH2COOH$��_{��}^{����}$
+H2O��C�������۷�Ӧ��m HOCH2CH2COOH$��_{��}^{����}$ +��m-1��H2O��
+��m-1��H2O��
�ٸ�����Ϣ����������Ȼ��ϵ��Ȼ���±Ԫ��ԭ��ȡ����������サ��±����±����һˮ��Ӧ�����Ը߷��ӻ����C4H5Cl��nΪ[CH2CH=CClCH2]n��C��Ũ����������·���������Ӧ������Ԫ������C��E��HOCH2CH2COOH$��_{��}^{Ũ����}$ +H2O������EΪ
+H2O������EΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��B��C�����ӳɷ�Ӧ����ӦΪ��OHCCH2CH2COOH+H2$\stackrel{����}{��}$HOCH2CH2COOH��
C�������۷�Ӧ��m HOCH2CH2COOH$��_{��}^{����}$ +��m-1��H2O��
+��m-1��H2O��
�ʴ�Ϊ��OHCCH2CH2COOH+H2$\stackrel{����}{��}$HOCH2CH2COOH��m HOCH2CH2COOH$��_{��}^{����}$ +��m-1��H2O���ӳɷ�Ӧ�����۷�Ӧ��
+��m-1��H2O���ӳɷ�Ӧ�����۷�Ӧ��
���� ���⿼���л����ƶϣ��ؼ��Ǹ���������Ϣ��������ת���������������ʽṹ���ƶϣ���Ŀ�Ѷ��еȣ�����ʱע����ݸ�����Ϣ̼̼˫����������Ӧ������п�۴�����ˮ��ת����ϵ���з����жϣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ������Ԫ��ԭ�ӵ���������������8 | |
| B�� | �ǽ���Ԫ�ص�����������������3 | |
| C�� | ����Ԫ�ص���������������С��4 | |
| D�� | ����ԭ�Ӻ˶��������Ӻ����ӹ��ɵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +2 | +6��-2 | -2 |
| A�� | �⻯��ķе�ΪH2T��H2R | |
| B�� | M��T�γɵĻ����������ǿ�ᷴӦ������ǿ�Ӧ | |
| C�� | �������Ũ�ȵ�ϡ���ᷴӦ�ľ��ҳ̶�ΪQ��L | |
| D�� | L2+��R2-����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A��B | B�� | B��C | C�� | C��D | D�� | D��E |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | $\frac{��a+c��}{��a+b��}$ | B�� | $\frac{��2c+a��}{��a+b+c��}$ | C�� | $\frac{2��a+c��}{��a+2b+c��}$ | D�� | $\frac{��2c+a��}{��2b+a��}$ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com