
【题目】由环己烷可制得1,4-环己二醇,流程如下(其中无机产物都已略去),试回答:

(1)反应_________属于取代反应(填反应序号).
(2)化合物的结构简式:B______________,C_______________.
(3)反应⑥所用试剂和条件是________________________.
(4)写出反应②、⑤的化学方程式:反应②________________反应⑤__________________.
【答案】(1)①⑥;
(2)B![]() ;C
;C![]() ;
;
(3)NaOH的水溶液、加热 ;
(4)②![]()
![]()
![]() +HCl;⑤
+HCl;⑤![]() +Br2
+Br2![]()
![]() 。
。
【解析】
试题分析: ![]() 与Cl2在光照时发生取代反应,产生
与Cl2在光照时发生取代反应,产生![]() ;该物质与NaOH的乙醇溶液发生消去反应,产生A是环己烯
;该物质与NaOH的乙醇溶液发生消去反应,产生A是环己烯![]() ;A与Cl2在不见光的作用下发生加成反应产生B是1,2-二氯环己烷
;A与Cl2在不见光的作用下发生加成反应产生B是1,2-二氯环己烷![]() ;B发生消去反应产生1,3-环己二烯
;B发生消去反应产生1,3-环己二烯![]() ;1,3-环己二烯与溴水按1:1发生加成反应产生
;1,3-环己二烯与溴水按1:1发生加成反应产生![]() ;
;![]() 与NaOH的水溶液在加热时发生取代反应,产生C:
与NaOH的水溶液在加热时发生取代反应,产生C:![]() ,该物质与氢气在一定条件下发生加成反应产生
,该物质与氢气在一定条件下发生加成反应产生![]() 。(1)上述反应中,①⑥属于取代反应;(2)化合物B的结构简式是
。(1)上述反应中,①⑥属于取代反应;(2)化合物B的结构简式是![]() ;化合物C的结构简式是
;化合物C的结构简式是![]() ;(3)反应⑥是卤代烃
;(3)反应⑥是卤代烃![]() 反应成为
反应成为![]() ,所用试剂和条件是NaOH的水溶液、加热;(4)反应②的化学方程式是:
,所用试剂和条件是NaOH的水溶液、加热;(4)反应②的化学方程式是:![]()
![]()
![]() +HCl;反应⑤
+HCl;反应⑤![]() +Br2
+Br2![]()
![]() 。
。


 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种新型能源,利用二氧化碳合成新能源已成为环保化学家研究的热门课题。
(1)几种共价键的键能如表所示:
化学键 | C=O | H-H | C-H | C-O | H-O |
键能/kJ·mol-1 | 803 | 436 | 414 | 326 | 464 |
2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ![]() _______________。
_______________。
(2)“人工光合作用”技术备受瞩目,该技术模拟事物的光合作用,利用太阳光将H2O和CO2直接合成燃料和化工原料。科研人员模拟光合作用,设计如图甲所示装置制备二甲醚。能量转化形式为太阳能![]() 电能
电能![]() 化学能、
化学能、
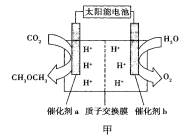
①催化剂b的电极名称是_________________。
②若释放11.2L氧气(标准状况下),有___________mol H+___________(填质子的迁移方向)。
③催化剂a上的电极反应式为______________。
(3)华盛顿大学的研究人员研究出一种方法,可实现水泥生产时CO2的零排放,其基本原理如图乙所示:
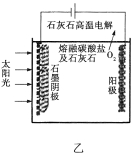
①生产过程中能量的转化形式是__________________。
②电解反应在温度小于900![]() 时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为_______________,阴极的电极反应式为______________。
时进行,碳酸钙分解为CaO和CO2,电解质为熔融碳酸钠,则阳极的电极反应式为_______________,阴极的电极反应式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科学家利用二氧化铈(CeO2)在太阳能作用下将H2O、CO2转变成H2、CO。其过程如下:mCeO2![]() (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xH2O+ xCO2![]() mCeO2+ xH2+ xCO
mCeO2+ xH2+ xCO
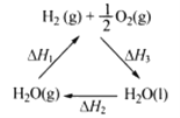
下列说法不正确的是( )
A.该过程中CeO2没有消耗
B.该过程实现了太阳能向化学能的转化
C.右图中△H1=△H2+△H3
D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH——2e—=CO32-+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应:2NO2![]() 2NO+O2 在恒容密闭容器中反应,达到平衡状态的标志是( )
2NO+O2 在恒容密闭容器中反应,达到平衡状态的标志是( )
①单位时间内生成n molO2的同时生成2n molNO2;
②单位时间内生成n molO2 的同时生成2n mol NO;
③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2:2:1的状态;
④混合气体中![]() 不变;
不变;
⑤混合气体的颜色不再改变的状态;
⑥混合气体的密度不再改变的状态;
⑦混合气体的平均相对分子质量不再改变的状态.
A.①⑤⑥ B.①④⑤⑦ C.①⑤⑥⑦ D.①③⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为___________;
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中![]() 为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
为:___________,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g)![]() H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
H2(g)+I2(g)的△H=+11kJmol-1,1molH2(g)、1molI2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为___________ kJ。
(4)Bodensteins研究了下列反应:2HI(g)![]() H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
H2(g)+I2(g),在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如表:
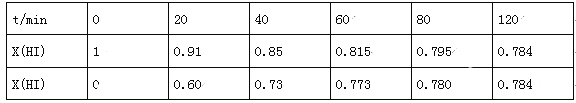
①根据上述实验结果,该反应的平衡常数K的计算式为:___________;
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为___________(以K和k正表示).若k正=0.0027min-1,在t=40min时,v正=___________min-1.
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用如图表示.当升高到某一温度时,反应重新达到平衡,相应的点分别为___________(填字母).
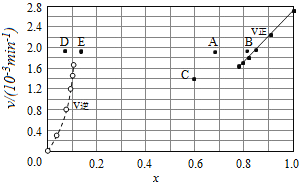
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.乙烯是是由裂解气的主要成分,它的产量通常用来衡量一个国家的石油化工水平。
下图是石蜡油在炽热碎瓷片的作用下产生乙烯并检验其性质的实验,完成下列问题。
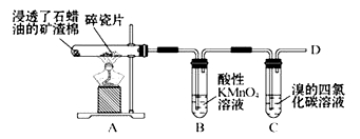
(1)A中碎瓷片的作用是 。
(2)B中反应类型是 。C中实验现象是 。
II.现有CH4、C2H4、C6H6三种有机化合物:
(3)等质量的以上物质完全燃烧时耗去O2的量最多的是__________。生成二氧化碳最多的是__________,生成水最多的是_________。
III.(4)分子式为C9H12的苯的同系物有 种,若在苯环上发生硝化反应时,生成的一硝基取代物只有一种,该烃的结构简式为 。
(5)分子中含有22 个共价键的烷烃,烷烃的分子式: 。
(6)支链只有一个乙基且式量最小的烷烃的结构简式 ,其名称为 。
(7)将某种烷烃进行氯代反应,测出一氯代物有4 种。3.6g 该烃完全生成一氯代物时,放出的气体用蒸馏水完全吸收,所得溶液用0.1 mol·L-1NaOH 溶液500mL恰好中和。则此烷烃的分子式为 ,其结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的综合利用对于改善大气质量和能源充分利用有重要的意义。
(1)下列说法正确的是 (填序号)。
a.煤是由有机物和少量无机物组成的复杂混合物
b.煤在燃烧过程中会生成一氧化碳、二氧化碳、氮氧化物、烟尘等有害物质
c.可利用生石灰、熟石灰、石灰石等固硫剂使煤在燃烧过程中生成稳定的硫酸盐
d.煤的干馏属于化学变化,煤的气化和液化都属于物理变化
(2)煤的气化过程中产生的有害气体H2S用氨水吸收生成正盐的离子方程式是
。
(3)燃煤烟气的一种脱硫方案-火碱-石灰-石膏法流程图1如下:
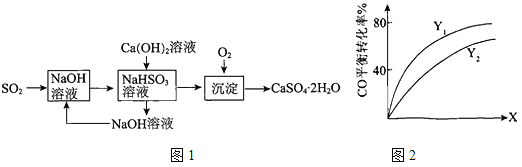
①常温下,用NaOH溶液吸收SO2得到pH=6的NaHSO3溶液,该溶液中离子浓度的大小顺序是
。
②氢氧化钙与NaHSO3反应的化学方程式是 。
(4)煤的间接液化法合成二甲醚的三步反应如下:
Ⅰ.2H2(g)+CO(g) ![]() CH3OH(g) △H=-90.8kJ·mol-1
CH3OH(g) △H=-90.8kJ·mol-1
Ⅱ.2CH3OH(g) ![]() CH3OCH3(g)+ H2O(g) △H=-23.5 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H=-23.5 kJ·mol-1
Ⅲ.CO(g) + H2O(g) ![]() CO2(g) + H2(g) △H=-41.3 kJ·mol-1
CO2(g) + H2(g) △H=-41.3 kJ·mol-1
① 总反应热化学方程式:3H2(g)+ 3CO(g) ![]() CH3OCH3(g)+ CO2(g) △H=
CH3OCH3(g)+ CO2(g) △H=
② Y(Y1、Y2),X可分别代表压强或温度。如图2表示Y一定时,总反应中CO的平衡转化率随X的变化关系。判断Y1、Y2的大小关系,并简述理由:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化锶晶体在工业上常用作铝的缓蚀剂。工业上一般用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体(SrCl2·6H2O)的过程为:

已知:Ⅰ.SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
Ⅱ. 有关氢氧化物开始沉淀和完全沉淀的pH如下表:
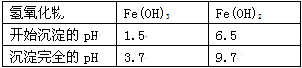
(1)操作①在实际工业生产中常常把碳酸锶粉碎并加以搅拌,其目的是 。碳酸锶与盐酸反应的化学方程式为 。
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为__________。能否用新制氯水代替双氧水 (填“能”或“否”)。
(3)在步骤②-③的过程中,将溶液的pH值由1调节至 ;宜用的试剂为 。
A.1.5 B.4 C.9.7
D.氨水 E.氢氧化锶粉末 F.碳酸钠晶体 G.氧化锶粉末
(4)操作③中所得滤渣的主要成分是 (填化学式)。
(5)工业上用50~60℃热风吹干六水氯化锶,选择该温度的原因是 。
(6)步骤⑥中,洗涤氯化锶晶体最好选用 。
A.水 B.稀硫酸 C.氢氧化钠溶液 D.氯化锶饱和溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列装置是用燃烧法确定有机物分子式常用的装置。
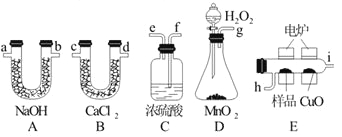
已知产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是g→f→e→h→i→c→d→a→b→f。
(1)C装置中浓硫酸的作用是________________________。
(2)D装置中MnO2的作用是_______________________。
(3)燃烧管中CuO的作用是_____________________。
(4)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,A管 质量增加1.76 g,B管质量增加1.08 g,则该样品的化学式为_________。
(5)若该物质的核磁共振氢谱如下图所示,
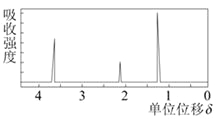
则其结构简式为___________________,该有机物的同分异构体结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com