
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为________mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________。
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液的密度
D.溶液中Cl-的数目
(3)下列容量瓶的使用方法中,不正确的是______。
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2 cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2 cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(4)某学生欲用上述浓盐酸和蒸馏水配制480 mL物质的量浓度为0.200 mol·L-1的稀盐酸。
①该学生需要用量筒量取________mL上述浓盐酸进行配制(精确到0.1)。
②在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏大的有________。
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.用量筒量取浓盐酸时俯视观察凹液面
C.在容量瓶中定容时俯视刻度线
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线
【答案】(1)11.9(3分) (2)BC(2分) (3)BCD(3分)
(4)①8.4(2分) ②C(3分)
【解析】(1)根据公式c=![]() ,该浓盐酸中HCl的物质的量浓度c=
,该浓盐酸中HCl的物质的量浓度c=![]() mol·L-1=11.9 mol·L-1。
mol·L-1=11.9 mol·L-1。
(2)溶液是均一、稳定的混合物,所以取用任意体积的该盐酸溶液时,根据n=cV可知,溶液中HCl的物质的量与溶液的体积有关系,A项错误;溶液的浓度是不变的,B项正确;溶液的密度是溶液的性质,与溶液的体积无关,C项正确;溶液中Cl-的数目与氯化氢的物质的量有关系,所以与溶液的体积有关,D项错误。
(3)容量瓶用水洗净后,不能用待配溶液洗涤,否则浓度偏高,B项错误;配制溶液时,试样要在烧杯中溶解,C项错误;配制溶液时,若试样是液体,用量筒取样后在烧杯中稀释冷却后再用玻璃棒引流转入容量瓶中,D项错误。
(4)①由稀释过程中溶质的物质的量不变可知配制500 mL 0.2 mol·L-1的稀盐酸需要该浓盐酸的体积为:![]() =0.008 4 L=8.4 mL。②根据cB=
=0.008 4 L=8.4 mL。②根据cB=![]() 可知,转移溶液后未洗涤烧杯和玻璃棒就直接定容,则导致盐酸的浓度偏小,A项错误;俯视量筒刻度线,则量筒中溶液的体积偏小,导致盐酸的浓度偏小,B项错误;在容量瓶中定容时俯视刻度线,则容量瓶中溶液的体积偏小,导致盐酸的浓度偏大,C项正确;定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,会使溶液体积增大,导致浓度偏小,D项错误。
可知,转移溶液后未洗涤烧杯和玻璃棒就直接定容,则导致盐酸的浓度偏小,A项错误;俯视量筒刻度线,则量筒中溶液的体积偏小,导致盐酸的浓度偏小,B项错误;在容量瓶中定容时俯视刻度线,则容量瓶中溶液的体积偏小,导致盐酸的浓度偏大,C项正确;定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线,会使溶液体积增大,导致浓度偏小,D项错误。


科目:高中化学 来源: 题型:
【题目】硅在能源、电子、信息等领域有重要应用,如用于制备太阳能电池。下列关于晶体硅的说法正确的是( )
A. 是一种半导体材料 B. 硬度小
C. 常温下化学性质活泼 D. 熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关钠的叙述正确的是
A.钠在空气中燃烧生成氧化钠
B.钠元素在自然界中可以以游离态形式存在
C.少量金属钠可以保存在煤油中
D.金属钠投入硫酸铜溶液中有铜生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近医学界通过用14C标记的C60发现一种C60的羧酸衍生物,在特定条件下可以通过断裂DNA抑制艾滋病毒的繁殖,则有关14C的正确叙述是( )
A. 与12C60的碳原子化学性质不同 B. 与14N含的中子数相同
C. 是12C60的同素异形体 D. 与12C、13C互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家发现了某种元素的一种新原子,其质量是a g,12C原子的质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是
A.由已知信息可得NA=![]()
B.w g该原子的物质的量一定是![]() mol
mol
C.w g该原子中含有![]() 个原子
个原子
D.该元素的摩尔质量是aNA g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 使用“乙醇汽油”、“燃煤固硫”、“汽车尾气催化净化”等可提高空气质量
B. 液氯、明矾净水原理相同
C. 硅胶和铁粉均可用于食品的防腐
D. 陶瓷、水泥和光导纤维均属于硅酸盐材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O5常用作纺织业棉麻脱氯剂;酸化时可放出SO2气体。其制备工艺流程
如下:
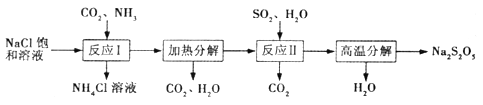
(1)Na2S2O5的名称为_______________(选填“焦硫酸钠”或“焦亚硫酸钠”)。
(2)“反应I ”中应先通入的气体是______,反应后析出的固体产物是____________。
(3)“反应II”的化学方程式为_________________________。
(4)若反应条件或用量等控制不当,则所得的Na2S2O5产品中往往含有杂质。
①若产品中含有杂质Na2SO3,其具体原因可能是______________(任答一条即可);
②若检验产品中含有杂质Na2SO3,下列试剂的使用顺序依次为_________(填编号)。
a.稀硫酸 b.澄淸石灰水 c.品红溶液 d.酸性KMnO4溶液
(5)Na2S2O3也可用作棉麻的脱氯剂。
①Na2S2O5溶液与Cl2反应的离子方程式为____________________;
②Na2S2O5与Na2S2O3脱氯等效时,消耗二者的质量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100 mL 1.5 mol·L1稀硫酸中加入过量Mg粉,充分反应后,滤去多余Mg粉,滤液在t ℃下恒温蒸发,当滤液质量为72.0 g时开始析出MgSO4·xH2O晶体,当析出晶体12.3 g时,剩下滤液48.0 g。通过计算回答下列问题。
(1)计算生成标准状况下的气体体积(请写出计算过程);
(2)开始析出MgSO4·xH2O晶体时溶液的质量分数为 ;
(3)MgSO4·xH2O中的x= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是几种常见的化学电源示意图,有关说法不正确的是( )

A. 上述电池分别属于一次电池、二次电池和燃料电池
B. 干电池在长时间使用后,锌筒被破坏
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 铅蓄电池工作过程中,每通过2mol电子,负极质量减轻207g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com