
| A. | NO HNO3 | B. | CH2=CH2 CH3CHO | C. | Fe FeCL3 | D. | Si H2SiO3 |
分析 A、一氧化氮氧化成二氧化氮,二氧化氮与水反应生成硝酸;
B、CH2=CH2与水加成生成乙醇,乙醇氧化成CH3CHO;
C、铁与盐酸生成氯化亚铁,氯化亚铁与氯气生成氯化铁;
D、硅氧化成二氧化硅,而二氧化硅无法转化为硅酸.
解答 解:A、一氧化氮氧化成二氧化氮,二氧化氮与水反应生成硝酸,三种物质之间能通过一步反应实现转化,故A正确;
B、CH2=CH2与水加成生成乙醇,乙醇氧化成CH3CHO,三种物质之间能通过一步反应实现转化,故B正确;
C、铁与盐酸生成氯化亚铁,氯化亚铁与氯气生成氯化铁,三种物质之间能通过一步反应实现转化,故C正确;
D、硅氧化成二氧化硅,而二氧化硅无法转化为硅酸,三种物质之间不能通过一步反应实现转化,故D错误;
故选D.
点评 本题综合考查物质的性质,为高频考点,把握物质的性质及相互转化发生的反应为解答的关键,注意一步转化为解答的易错点,选项D中二氧化硅不溶于水也不与水反应是解答的难点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 弱电解质在溶液中部分电离,存在电离平衡 | |
| B. | 同一弱电解质的溶液,当温度或浓度不同时,其导电能力也不相同 | |
| C. | 电离常数(K)越小,表示弱电解质电离能力越弱 | |
| D. | 不同浓度的同一弱电解质,其电离常数(K)不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 铜锌原电池(如图)工作时,以下说法正确的是( )
铜锌原电池(如图)工作时,以下说法正确的是( )| A. | ①②③ | B. | ②④⑤ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
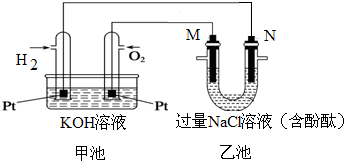 如图所示是氢氧燃料电池工作时的装置,乙池中的两个电极均是石墨电极,请回答下列问题:
如图所示是氢氧燃料电池工作时的装置,乙池中的两个电极均是石墨电极,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 制备AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 | |
| B. | 在镀件上电镀锌,用锌作阳极 | |
| C. | 用如图1装置生产家用消毒液(NaClO) | |
| D. | 用如图2装置为铅蓄电池充 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与氧气 | B. | 澄清石灰水与二氧化碳 | ||
| C. | Al与稀盐酸 | D. | KHCO3与Ba(OH)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com