
用如图所示装置制取表格中的四种干燥、纯净的气体(必要时可以加热;a、b、c、d表示相应仪器中加入的试剂)。其中正确的是 ( )。
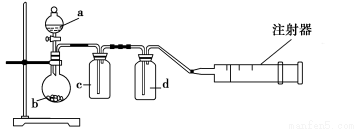
选项 | 气体 | a | b | c | d |
A | SO2 | 浓硫酸 | Cu | H2O | 浓硫酸 |
B | Cl2 | 浓盐酸 | MnO2 | NaOH溶液 | 浓硫酸 |
C | NH3 | 饱和NH4Cl溶液 | 消石灰 | 空集气瓶 | 固体NaOH |
D | NO | 稀硝酸 | 铜屑 | H2O | 浓硫酸 |
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案科目:高中化学 来源:2014年高考化学题型冲刺练习 化学基本概念、解决化学与STSE问题(解析版) 题型:选择题
我国稀土矿资源丰富,品位甚高。提取稀土元素可以向含RE(RE表示稀土元素)的硫酸盐溶液中加入粉状Na2SO4,使稀土元素转入沉淀。有关的反应为(RE)2(SO4)3+Na2SO4+xH2O (RE)2(SO4)3·Na2SO4·xH2O↓。下列叙述不正确的是( )
(RE)2(SO4)3·Na2SO4·xH2O↓。下列叙述不正确的是( )
A.该反应属于化合反应
B.该反应属于可逆反应
C.生成的产物在分类上属于复盐
D.RE在化合物中的化合价为+3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练4 无机化工流程题专项突破练习卷(解析版) 题型:填空题
废旧硬质合金刀具中含碳化钨(WC)、金属钴(Co)及少量杂质铁,利用电解法可回收WC和Co。工艺流程简图如下:
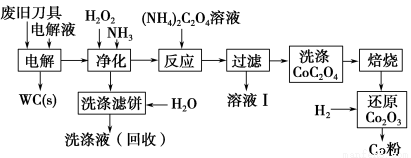
(1)电解时废旧刀具做阳极,不锈钢做阴极,HCl溶液为电解液。阴极主要的电极反应式为 。
(2)净化步骤所得滤饼的主要成分是 。回收的洗涤液代替水配制电解液,目的是回收利用其中的 。
(3)溶液Ⅰ的主要成分是 。洗涤CoC2O4不充分对最终产品纯度并无明显影响,但焙烧时会造成环境污染,原因是 。
(4)将Co2O3还原成Co粉的化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练2 阿伏加德罗常数的判断练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是( )。
A.1 L 0.1 mol·L-1的氨水中含有的NH3分子数为0.1 NA
B.标准状况下,2.24 L的CCl4中含有的C—Cl键数为0.4 NA
C.常温常压下,3.0 g含甲醛的冰醋酸中含有的原子总数为0.4 NA
D.常温常压下,Na2O2与足量CO2反应生成2.24 L O2,转移电子数为0.2 NA
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习专练1 化学实验仪器的创新使用练习卷(解析版) 题型:填空题
某校化学研究性学习小组,在学习金属的冶炼以后对一氧化碳还原金属氧化物的实验非常感兴趣,他们查阅有关资料后发现,一氧化碳的制备可利用甲酸和浓硫酸共热到60~80 ℃发生脱水反应制取:
HCOOH CO↑+H2O
CO↑+H2O
请根据以下各图帮他们组装成一套相对合理的实验装置图(某些装置可重复使用)。
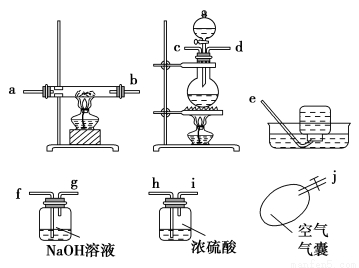
回答以下问题:
(1)合理实验装置的连接顺序是(写小写字母) 。
(2)在反应时一定要先通一会一氧化碳气体,然后再点燃加热氧化铁的酒精灯,原因是 。
A.因为一般反应从左到右进行
B.排除体系内的空气,使反应过程更安全
C.甲酸与浓硫酸反应可以产生大量的CO
D.此反应加热时间长有利于产生CO
(3)请说出你所选择的第一个NaOH洗气瓶的作用是 。
(4)在观察到硬质玻璃管中的物质由 色完全变为 色时停止加热,然后继续 ,原因是防止铁被氧化。
(5)硬质玻璃管中发生反应的化学方程式为 。
(6)该实验的一个优点是把实验过程中的尾气利用排水法收集起来,收集的气体前后有几瓶,分别按收集的先后顺序编号,点燃各个瓶中的气体,中间编号的集气瓶中气体 ,编号最先和最后的集气瓶中气体 ,原因是 。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第3章 物质在水溶液中的行为练习卷(解析版) 题型:填空题
10℃时加热饱和NaHCO3溶液,测得该溶液的pH发生如表所示的变化。
温度/℃ | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
甲同学认为,该溶液pH增大的原因是HCO 的水解程度增大,故碱性增强,有关反应的离子方程式为__________________________。乙同学认为,溶液pH增大的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度________(填“大于”或“小于”)NaHCO3的水解程度,该分解反应的化学方程式为______________________________。
的水解程度增大,故碱性增强,有关反应的离子方程式为__________________________。乙同学认为,溶液pH增大的原因是NaHCO3受热分解生成了Na2CO3,并推断Na2CO3的水解程度________(填“大于”或“小于”)NaHCO3的水解程度,该分解反应的化学方程式为______________________________。
丙同学认为,甲、乙的判断都不充分,他进行如下探究来验证他们的判断是否正确。
(1)在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则________(填“甲”或“乙”)的判断正确,试剂X是________(填序号)。
A.Ba(OH)2溶液 B.BaCl2溶液
C.NaOH溶液 D.澄清石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH________(填“大于”“小于”或“等于”)8.3,则________(填“甲”或“乙”)的判断正确。
(3)丙同学查阅资料后发现,NaHCO3的分解温度为150℃,他断言________(填“甲”或“乙”)的判断是错误的,原因是________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第3章 物质在水溶液中的行为练习卷(解析版) 题型:选择题
如图所示用一定浓度的NaOH溶液Y滴定10 mL一定物质的量浓度的盐酸X,依据图示推出X和Y的物质的量浓度是下列各组中的( )
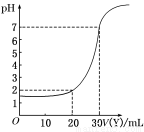
| A | B | C | D |
X物质的量浓度/mol·L-1 | 0.12 | 0.04 | 0.03 | 0.09 |
Y物质的量浓度/mol·L-1 | 0.04 | 0.12 | 0.09 | 0.03 |
查看答案和解析>>
科目:高中化学 来源:2014年高中化学鲁科版选修四第1章 化学反应与能量转化练习卷(解析版) 题型:填空题
将1 L含有0.4 mol CuSO4和0.2 mol NaCl 的水溶液用惰性电极电解一段时间后。
(1)若在一个电极上得到0.1 mol Cu,另一电极上析出气体(在标准状况下)的体积是________ L。
(2)若在一个电极上恰好得到0.4 mol Cu,另一电极上再析出气体(在标准状况下)的体积是________ L。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学苏教版选修四专题3 溶液中的离子反应练习卷(解析版) 题型:填空题
现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是____________。
(3)已知t°C,KW=1×10-13,则t°C______(填“>”、“<”或“=”)25°C。
(4)25°C时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和。两溶液的pH(x、y)的关系式为________________(填表达式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com