
【题目】回答下列问题。
(1)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质,下面给出14种元素的电负性。
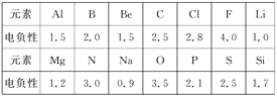
①判断下列化合物中属于离子化合物的是________(填字母);
A.Mg3N2 B.BeCl2 C.AlCl3 D.SiC
②已知PCl3、NCl3均能发生水解反应,PCl3水解反应的化学方程式为__________________________;NCl3水解产物为____________________。
(2)观察Li、Be、Mg、Al在元素周期表中的位置回答:
![]()
①铍的最高价氧化物的水化物是________(填“酸性”、“碱性”或“两性”)化合物,证明这一结论的有关离子方程式是_____________________________________________________;
②根据Mg在空气中的燃烧情况,Li在空气中燃烧生成产物为__________(用化学式表示)。
(3)现有核电荷数小于20的元素A,其电离能数据如下:(I1表示原子失去第1个电子的电离能;In表示原子失去第n个电子的电离能,单位:1×102kJ·mol-1)

①外层电子离核越远,能量越高,电离能越__________(填“大”或“小”);阳离子电荷数越高,失去电子时,电离能越________(填“大”或“小”);
②上述11个电子分属________个电子层;
③失去了11个电子后,该元素还有________个电子;
④该元素最高价氧化物对应水化物的化学式是______________________________________。
【答案】A PCl3+3H2O=H3PO3+3HCl HClO、NH3·H2O 两性 Be(OH)2+2OH-=BeO22-+2H2O、Be(OH)2+2H+=Be2++2H2O Li2O、Li3N 小 大 3 1 Mg(OH)2
【解析】
(1)①根据形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键分析;
②PCl3、NCl3均能发生水解反应,结合元素化合价分析水解产物;
(2)①铍的最高价氧化物的水化物是两性化合物;两性化合物与强酸、强碱均反应生成盐和水;
②Mg和Li相似,Mg在空气中燃烧生成MgO和Mg3N2;
(3)同一种元素的原子,其电离能随着失电子个数的增多而增大,当原子失去电子变为稳定状态时,如果继续失电子,则其电离能会出现突兀性变化,据此判断该元素最外层电子数,据此解答。
(1)①A.Mg3N2电负性差值为3.0-1.2=1.8,大于1.7形成离子键,属于离子化合物;
B.BeCl2电负性差值为3.0-1.5=1.5,小于于1.7形成共价键,属于共价化合物;
C.AlCl3电负性差值为3.0-1.5=1.5,小于于1.7形成共价键,属于共价化合物;
D.SiC电负性差值为2.5-1.8=0.7,小于于1.7形成共价键,属于共价化合物;
故答案为A;
②水解反应前后各元素的化合价不变,Cl的电负性大于P,所以在PCl3中P为+3价,Cl为-1价,则在PCl3水解的产物中P元素的化合价是+3价,Cl元素的化合价是-1价,PCl3水解反应的化学方程式为PCl3+3H2O=H3PO3+3HCl;水解反应前后各元素的化合价不变,由题意知NCl3中N的化合价为-3价,Cl的化合价为+1价,则在NCl3水解的产物中N的化合价是-3价,Cl的化合价是+1价,其水解产物是HClO和NH3·H2O;
(2)①铍和铝的性质相似,铝的最高价氧化物的水化物是两性化合物,则铍的最高价氧化物的水化物是两性化合物;两性化合物与强酸、强碱均反应生成盐和水,离子反应分别为Be(OH)2+2H+═Be2++2H2O、Be(OH)2+2OH-═BeO22-+2H2O;
②Mg和Li相似,Mg在空气中燃烧生成MgO和Mg3N2,所以Li在空气中燃烧生成的产物为Li2O和Li3N;
(3)①外层电子离核越远,能量越高,失去外层电子越容易,电离能越小;阳离子电荷数越高,再失去电子就越因难,电离能越大;
②根据核外电子排布可知11个电子应排为:1s22s22p63s1,则这11个电子分属3个电子层;
③根据失去第一个、第二个电子的能量比失去第三个电子的能量小很多,得知该元素易失去2个电子,又因该元素可以失去的电子能达到11个,故在前20号中只有镁符合要求,镁是12号元素,失去11个电子后,还有1个电子;
④镁的最高价为+2价,其氧化物MgO对应水化物的化学式是Mg(OH)2。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】已知化学反应2C(s)+O2(g)![]() 2CO(g);2CO(g)+O2(g)
2CO(g);2CO(g)+O2(g)![]() 2CO2(g)都是放热反应。据此推断在相同条件下,下列说法不正确的是( )
2CO2(g)都是放热反应。据此推断在相同条件下,下列说法不正确的是( )
A.56 g CO和32 g O2所具有的总能量之和大于88 g CO2所具有的总能量
B.12 g C所具有的能量一定高于28 g CO所具有的能量
C.12 g C和32 g O2所具有的总能量大于44 g CO2所具有的总能量
D.将两份质量相等的碳完全燃烧,生成CO2的反应比生成CO的反应放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,给一氧化碳和水蒸气的气体混合物加热,在催化剂存在下发生反应:CO(g)+H2O(g)![]() H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
H2(g)+CO2(g)。在500 ℃时,平衡常数K=9。若反应开始时,一氧化碳和水蒸气的浓度都是0.02 mol/L,则在此条件下CO的转化率为( )
A. 25% B. 50% C. 75% D. 80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以芳香烃A为原料发生如图所示的变化,可以合成高聚物G。
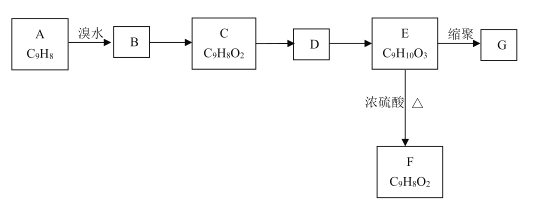
已知:①两个羟基连在同一碳原子上不稳定,会自动脱水。
②C能发生银镜反应,F能使溴水褪色。
回答下列问题:
(1)A中官能团的名称是________;C的结构简式为_________。
(2)B→C的反应条件是________,E→F的反应类型是_________。
(3)写出E→G的化学方程式________。
(4)E的同分异构体中,苯环上有4个取代基、遇FeCl3溶液显紫色且能与碳酸氢钠溶液反应的共有________种(不考虑立体异构)。其中核磁共振氢谱显示有4组峰的结构简式为________(写出一种即可)。
(5)参照上述合成路线,设计以丙炔为原料制备乳酸(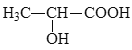 )的合成路线________(无机试剂任选)。
)的合成路线________(无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是

A. H2 B. CH3CH2OH(气) C. CO2 D. CO和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室合成乙酸乙酯的步骤如下:在图甲的圆底烧瓶内加入乙醇、浓硫酸和乙酸,加热回流一段时间,然后换成图乙装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。
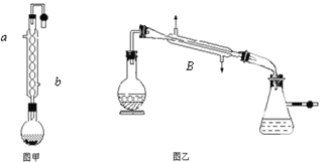
请回答下列问题
(1)图甲中冷凝水从______(a或b)进,图乙中B装置的名称为_______;
(2)图甲在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入沸石,目的是_______;
(3)反应中加入过量的乙醇,目的是_______;
(4)现拟分离粗产品乙酸乙酯、乙酸和乙醇的混合物下列框图是分离操作步骤流程图:
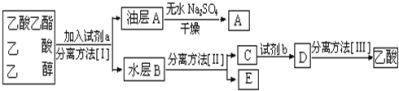
则试剂a是______,分离方法I是_______,分离方法II是_______,产物E是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分),设计了如下流程:
下列说法不正确的是
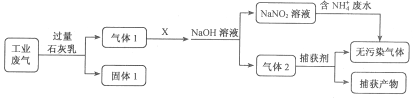
A. 固体1中主要含有Ca(OH)2、CaCO3、CaSO3
B. X可以是空气,且需过量
C. 捕获剂所捕获的气体主要是CO
D. 处理含NH4+废水时,发生反应的离子方程式为:NH4++NO2-==N2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家哈伯在合成氨方面的研究促进了人类的发展。合成氨的工业流程如图,下列说法错误的是
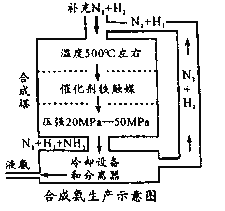
A.增大压强既可以加快反应速率,又可以提高原料转化率
B.升高温度可提高平衡转化率
C.冷却过程中采用热交换有助于节约能源
D.原料循环可提高其利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚磷酸(H3PO3)是二元弱酸,主要用于农药中间体以及有机磷水处理药剂的原料。常温下,向1L0.500mol·L-1H3PO3溶液中滴加等浓度的NaOH溶液,混合溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示,下列说法正确的是
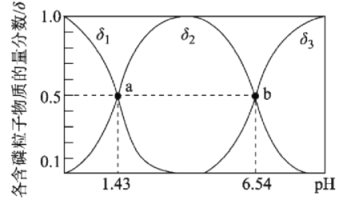
A.a、b两点时,水电离出的c水(OH-)之比为1.43:6.54
B.b点对应溶液中存在:c(Na+)=3c(HPO32-)
C.反应H3PO3+HPO32-![]() 2H2PO3-的平衡常数为105.11
2H2PO3-的平衡常数为105.11
D.当V(NaOH)=1 L 时,c(Na+)>c(H2PO3-)>c(OH-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com