
【题目】Q、W、X、Y、Z五种短周期元素在周期表中的相对位置如下图所示,其中W的单质是一种重要半导体材料。
|
|
| Y |
|
Q | W | X |
| Z |
请按要求回答下列问题:
(1)Y的原子结构示意图为________;举一例说明Z的非金属性比X的非金属性强的事实:________。
(2)W、X、Y的原子半径由大到小依次![]() 填元素符号
填元素符号![]() ________:W与Z形成的化合物电子式为________。
________:W与Z形成的化合物电子式为________。
(3)将Z的单质通入到含等物质的量FeBr2溶液中充分反应的离子方程式为________。
(4)已知: 2Na(s)+![]() Y2(g)=Na2Y(s)H=-414kJ/mol;2Na(s)+Y2(g)=Na2Y2(s)H=-511kJ/mol;则Na2Y(s)转变为Na2Y2(s)的反应一定条件下能自发进行的理由是________。将0.2mol Na2Y2加入到100mL1mol/L的QZ3中,充分反应的化学方程式为________。
Y2(g)=Na2Y(s)H=-414kJ/mol;2Na(s)+Y2(g)=Na2Y2(s)H=-511kJ/mol;则Na2Y(s)转变为Na2Y2(s)的反应一定条件下能自发进行的理由是________。将0.2mol Na2Y2加入到100mL1mol/L的QZ3中,充分反应的化学方程式为________。
(5)R与W同周期,已知:在T℃时Ksp[R(OH)2]的值为4.0×10-12,则R(OH)2饱和溶液中c(OH-)=________mol/L。
【答案】 酸性强弱:HClO4>H3PO4 r(Si)>r(P)>r(O)
酸性强弱:HClO4>H3PO4 r(Si)>r(P)>r(O) ![]() 2Fe2++2 Br-+2Cl2=2Fe3++Br2+4Cl- Na2O(s)+
2Fe2++2 Br-+2Cl2=2Fe3++Br2+4Cl- Na2O(s)+![]() O2(g)=Na2O2(s)H=-97kJ/mol,而S <0,H-TS <0时,反应可自发进行 2 Na2O2+ AlCl3= NaAlO2+3NaCl+ O2↑ 2.0×10-4
O2(g)=Na2O2(s)H=-97kJ/mol,而S <0,H-TS <0时,反应可自发进行 2 Na2O2+ AlCl3= NaAlO2+3NaCl+ O2↑ 2.0×10-4
【解析】
由短周期元素的相对位置,可知Y处于第二周期,其它处于第三周期,而W的单质是一种重要半导体材料,则W为Si元素,可推知Q为Al,X为P,Y为O,Z为Cl。
(1)Y为O元素,原子结构示意图为:![]() ,酸性强弱:HClO4>H3PO4,或稳定性:HCl>PH3等都可以说明Cl的非金属性比P的强;
,酸性强弱:HClO4>H3PO4,或稳定性:HCl>PH3等都可以说明Cl的非金属性比P的强;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:r(Si)>r(P)>r(O),W与Z形成的化合物为SiCl4,Si原子与每个Cl原子之间都形成1对共用电子对,电子式为: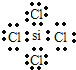 ;
;
(3)假设氯气与FeBr2均为1mol,还原性Fe2+>Br-,氯气先氧化Fe2+为Fe3+,根据电子转移守恒,1mol Fe2+消耗0.5mol氯气,而剩余的0.5mol氯气可以氧化1mol Br-,反应离子方程式为2Fe2++2 Br-+2Cl2=2Fe3++Br2+4Cl- ;
![]() 已知:①2Na(s)+
已知:①2Na(s)+![]() O2(g)=Na2O(s)H=-414kJ/mol;②2Na(s)+O2(g)=Na2O2(s)H=-511kJ/mol;根据盖斯定律,②-①可得:Na2O(s)+
O2(g)=Na2O(s)H=-414kJ/mol;②2Na(s)+O2(g)=Na2O2(s)H=-511kJ/mol;根据盖斯定律,②-①可得:Na2O(s)+![]() O2(g)=Na2O2(s)H=-97kJ/mol,该反应S<0,而H-TS <0时,反应可自发进行,故低温下可以自发进行,将0.2mol Na2O2加入到100mL1mol/L的AlCl3中,AlCl3为0.1mol,过氧化钠与水反应生成0.4molNaOH,氯化铝与氢氧化钠恰好反应生成NaAlO2,故反应方程式为:2 Na2O2+ AlCl3= NaAlO2+3NaCl+ O2↑;
O2(g)=Na2O2(s)H=-97kJ/mol,该反应S<0,而H-TS <0时,反应可自发进行,故低温下可以自发进行,将0.2mol Na2O2加入到100mL1mol/L的AlCl3中,AlCl3为0.1mol,过氧化钠与水反应生成0.4molNaOH,氯化铝与氢氧化钠恰好反应生成NaAlO2,故反应方程式为:2 Na2O2+ AlCl3= NaAlO2+3NaCl+ O2↑;
(5)Ksp[R(OH)2]=c(R2+)×c2(OH-)=4.0×10-12,而饱和溶液中c(R2+)=![]() c(OH-),联立可得饱和溶液中c(OH-)=2.0×10-4。
c(OH-),联立可得饱和溶液中c(OH-)=2.0×10-4。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】如图两圆相交部分A、B、C、D分别表示两物质间的反应。下列各对应反应的离子方程式书写不正确的是( )
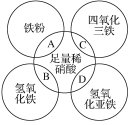
A.Fe+4H++NO3-=Fe3++NO↑+2H2O
B.Fe(OH)3+3H+=Fe3++3H2O
C.Fe3O4+8H+=Fe2++2Fe3++4H2O
D.3Fe(OH)2+10H++NO3-=3Fe3++NO↑+8H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】麻黄素M是拟交感神经药。合成M的一种路线如图所示:
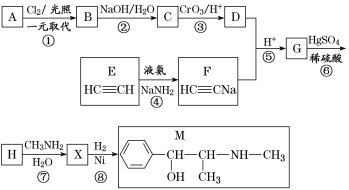
已知:Ⅰ.芳香烃A的相对分子质量为92
Ⅱ.R—CH2OH![]() RCHO
RCHO
III、R1-CHO+
IV、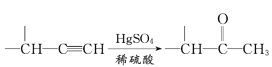
V、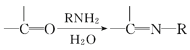
请回答下列问题:
(1)D的名称是_______;G中含氧官能团的名称是_______。
(2)反应②的反应类型为_______;A的结构简式为_______。
(3)写出反应⑦的化学方程式:______________________________。
(4)X分子中最多有_______个碳原子共平面。
(5)在H的同分异构体中,同时能发生水解反应和银镜反应的芳香族化合物中,核磁共振氢谱上有4组峰,且峰面积之比为1∶1∶2∶6的有机物的结构简式为_________________。
(6)已知:![]() 仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体
仿照上述流程,设计以苯、乙醛为主要原料合成某药物中间体![]() 的路线________________。
的路线________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)已知X、Y、Z、M、G、Q是六种短周期元素,原子序数依次增大。X、Z、Q的单质在常温下呈气态;Y的原子最外层电子数是其电子层数的2倍;X与M同主族;Z、G分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)Y、Z、M、G四种元素原子半径由大到小的顺序是(写元素符号) 。
(2)Z在元素周期表中的位置为 。
(3)上述元素的最高价氧化物对应的水化物酸性最强的是(写化学式) 。
(4)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质是(写分子式) ,在实验室中,制取该物质的反应原理是(写化学方程式) 。
(5)M2Z的电子式为 。MX与水反应可放出气体,该反应的化学方程式为 。
(6)常温下,不能与G的单质发生反应的是(填序号) 。
a.CuSO4溶液 b.Fe2O3c.浓硫酸 d.NaOH溶液 e.Na2CO3固体
工业上用电解法制G的单质的化学方程式是 ,若以石墨为电极,阳极产生的混合气体的成分是(写化学式) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应的离子方程式书写正确的是( )
A.氯化铝溶液与过量氨水反应:3NH3H2O+Al3+=Al(OH)3↓+3NH4+
B.向氢氧化钠溶液中通入过量的CO2气体:CO2+2OH-=CO32-+H2O
C.FeCl3溶液与Cu粉反应:Cu+Fe3+=Cu2++Fe2+
D.氢氧化钡溶液与稀硫酸反应:Ba2++SO42-+H++OH-=BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验题:Ⅰ.下列实验设计或操作合理的是____________。
A.在催化剂存在的条件下,苯和溴水发生反应可生成无色比水重的液体溴苯
B.只用水就能鉴别苯、硝基苯、乙醇
C.实验室制取乙烯时温度计的水银球在反应液上方
D.将10滴溴乙烷加入1 mL10%的烧碱溶液中加热片刻后,再滴加2滴2%的硝酸银溶液,以检验水解生成的溴离子
E.工业酒精制取无水酒精时先加生石灰然后蒸馏,蒸馏必须将温度计的水银球插入反应液中,测定反应液的温度
F.苯酚中滴加少量的稀溴水,可用来定量检验苯酚
G.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验
Ⅱ.学习卤代烃的性质时,张老师通过实验的方法验证溴乙烷在不同溶剂中与NaOH 反应生成不同的反应产物,请你一起参与他们的探究。
(1)张老师用如图所示装置进行实验:该实验的目的是__________;课上你所观察到的现象是_____;盛水试管(装置)的作用是________。
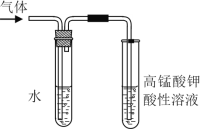
(2)若你用另一实验来达到张老师演示实验的目的,你设计的实验方案依据的反应原理是________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。请回答下列问题:
(1)PM2.5分散在空气中形成的分散系__(填“属于”或“不属于”)胶体。
(2)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
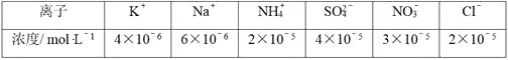
根据表中数据判断待测试样为__(填“酸”或“碱”)性,表示该试样酸碱性的c(H+)或c(OH-)=__mol·L-1。
(3)煤燃烧排放的烟气含有SO2和NOx,形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可对烟气进行脱硫,脱硝,效果非常好。完成下列对烟气脱硝过程的离子方程式。
__ClO2-+__NO+__=__Cl-+__NO3-+__
(4)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。写出焦炭与水蒸气反应的化学方程式:__。
②洗涤含SO2的烟气。以下物质可做洗涤剂的是__(填字母)。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(5)汽车尾气中NOx和CO的生成及转化。
①汽车启动后,汽缸温度越高,单位时间内NO排放量越大,写出汽缸中生成NO的化学方程式:__。
②汽车燃油不完全燃烧时产生CO,目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度氧化铝有广泛的用途,某研究小组研究用以下流程制取高纯度氧化铝:
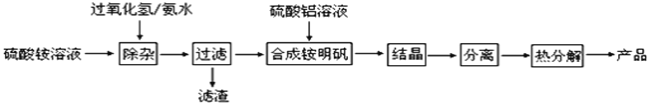
(1)“除杂”操作是加入H2O2后,然后用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中少量的Fe2+。
①酸性溶液中Fe2+与H2O2反应的离子方程式为___。
②过滤操作中所得到滤渣主要成分的化学式为___。
(2)检验上述流程中“过滤”后杂质是否除尽的实验方法___。
(3)配制硫酸铝溶液时,需用硫酸酸化的目的是___。
(4)“结晶”操作中,得到铵明矾晶体(NH4Al(SO4)212H2O),采用的操作是___。
(5)铵明矾晶体的化学式为NH4Al(SO4)212H2O,在0.1mol/L铵明矾的水溶液中,c(NH4+)、c(Al3+)、c(SO42﹣)三种离子浓度由大到小的顺序为___。
Kb(NH3·H2O)=1.8×10-5KbAl(OH)3=1.38×10-9
(6)向铵明矾溶液中加入过量NaOH溶液,反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数值。下列说法正确的是
A.12g![]() 的原子核内中子数为6NA
的原子核内中子数为6NA
B.9.0g葡萄糖和蔗糖的混合物中含碳原子的数目为0.3NA
C.25℃时,1LpH=2的H2C2O4溶液中含H+的数目为0.02NA
D.标准状况下,2.24LCO2与足量Na2O2反应转移的电子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com