
|
将由a mol NaHCO3和b mol NaOH组成的固体混合物放在密闭容器中加热到250℃,经充分反应后,排出气体,冷却后,称量残留固体的质量为W g,试计算W的值可能为 ①84a+40b ②53a+40b ③66a+40b ④53(a+b) | |
| [ ] | |
A. |
①② |
B. |
②④ |
C. |
只有④ |
D. |
③④ |
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源:江西省白鹭洲中学2009-2010学年高二3月月考化学试题 题型:022
二氧化硫和氮的氧化物是常用的工业原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
(1)硫酸生产中,SO2催化氧化成SO3:2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
某温度下,SO2的平衡转化率(α)与体系总压强(P)的关系如下图所示.根据图示回答下列问题:

①将2.0 mol SO2和1.0 mol O2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10 MPa.该反应的平衡常数等于________.
②平衡状态由A变到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”).
(2)用CH4催化还原NOx可以消除氮氧化物的污染.例如
:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1
若用标准状况下4.48 L CH4还原NO2
至N2,整个过程中转移的电子总数为________(阿伏加德罗常数用NA表示),放出的热量为________kJ.查看答案和解析>>
科目:高中化学 来源:2010年高三备考“好题速递”系列(18)化学试题 题型:022
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g).某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.根据图示回答下列问题:
2SO3(g).某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.根据图示回答下列问题:
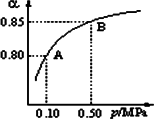
①将2.0 mol SO2和1.0 mol O2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10 MPa.该反应的平衡常数等于________.
②平衡状态由A变到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”)
(2)用CH4催化还原NOx可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)![]() 4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ/mol
4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ/mol
CH4
(g)+4NO(g)若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为________(阿伏加德罗常数的值用NA表示),放出的热量为________kJ.
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去.转化流程如图所示:
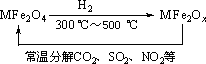
请写出MFe2Ox分解SO2的化学方程式________(不必配平)
查看答案和解析>>
科目:高中化学 来源:志鸿系列全优设计必修一化学鲁科版 鲁科版 题型:021
|
已知mg由Na2CO3、NaHCO3和Na2CO3·10H2O组成的混合物,将其全部溶于水后形成溶液,测得溶液中含有1 mol Na+,然后将溶液加热蒸干到质量不再变化为止,最终所得固体的质量是 | |
A. |
106 g |
B. |
53 g |
C. |
26.5 g |
D. |
m g |
查看答案和解析>>
科目:高中化学 来源:汕头市六都中学高三级2007-2008化学模拟试卷 题型:022
二氧化硫和氮的氧化物是常用的化工原料,但也是大气的主要污染物.综合治理其污染是环境化学当前的重要研究内容之一.
(1)硫酸生产中,SO2催化氧化生成SO3:2SO2(g)+O2(g)![]() 2SO3(g).某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.根据图示回答下列问题:
2SO3(g).某温度下,SO2的平衡转化率(α)与体系总压强(p)的关系如图所示.根据图示回答下列问题:
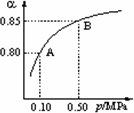
①将2.0 mol SO2和1.0 mol O2置于10 L密闭容器中,反应达平衡后,体系总压强为0.10 MPa.该反应的平衡常数等于________.
②平衡状态由A变到B时,平衡常数K(A)________K(B)(填“>”、“<”或“=”).
(2)用CH4催化还原NOx可以消除氮氧化物的污染.例如:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);Δ=-574 kJ/mol
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ/mol
若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为________(阿伏加德罗常数的值用NA表示),放出的热量为________kJ.
(3)新型纳米材料氧缺位铁酸盐(MFe2Ox,3<x<4,M=Mn、Co、Zn或Ni)由铁酸盐(MFe2O4)经高温还原而得,常温下,它能使工业废气中的酸性氧化物分解除去.转化流程如图所示:
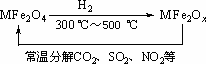
请写出MFe2Ox分解SO2的化学方程式________(不必配平).
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 Na2S4+3NaBr
Na2S4+3NaBr查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com