
| A. | 聚丙烯的链节是-CH2-CH2-CH2- | |
| B. | 向苯酚溶液中滴加Na2CO3溶液:2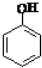 +CO${\;}_{3}^{2-}$→ +CO${\;}_{3}^{2-}$→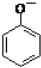 +CO2↑+H2O +CO2↑+H2O | |
| C. | 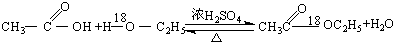 | |
| D. | 苯的同系物能使酸性高锰酸钾溶液褪色,说明烃基对苯环的性质产生了较大的影响 |
分析 A、聚丙烯的链节是-CH2-CH(CH3)-;
B、苯酚的酸性弱于碳酸;
C、酯化反应的实质是酸脱-OH醇脱-H;
D、苯的同系物能使酸性高锰酸钾溶液褪色,是高锰酸钾溶液将苯环侧链氧化的原因.
解答 解:A.聚丙烯的链节是-CH2-CH(CH3)-,故A错误;
B、苯酚的酸性弱于碳酸,但弱于HCO3-,故向苯酚溶液中滴加Na2CO3溶液,只能生成HCO3-: +CO${\;}_{3}^{2-}$→
+CO${\;}_{3}^{2-}$→ +HCO3-,故B错误;
+HCO3-,故B错误;
C、酯化反应的实质是酸脱-OH醇脱-H,故CH3CH218OH中的18O将到水中,故方程式为: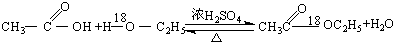 ,故C正确;
,故C正确;
D、苯的同系物能使酸性高锰酸钾溶液褪色,是由于高锰酸钾溶液将苯环侧链氧化为羧基,说明苯环使侧链活化,故D错误.
故选C.
点评 本题考查了化学方程式的书写,应注意的是苯酚的酸性弱于碳酸,但弱于HCO3-,故向苯酚溶液中滴加Na2CO3溶液,只能生成HCO3-.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
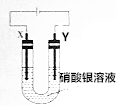 X、Y均为石墨电极,电解硝酸银溶液,实验装置如图所示,电解实验过程中,发现Y极增重的同时,Y极负极产生气泡且气泡由无色变红棕色.已知电流效率等于生成目标产物消耗电子书与电路转移总电子数之比.下列推断正确的是( )
X、Y均为石墨电极,电解硝酸银溶液,实验装置如图所示,电解实验过程中,发现Y极增重的同时,Y极负极产生气泡且气泡由无色变红棕色.已知电流效率等于生成目标产物消耗电子书与电路转移总电子数之比.下列推断正确的是( )| A. | Y极附近产生的无色气泡是H2 | |
| B. | X极附近电解质溶液中c(H+)会减小 | |
| C. | 若产生2.24L O2(标准状况下)时析出32.4g银,则电流效率为80% | |
| D. | 阴极的副反应为NO3-+3e-+4H+═NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 5种 | C. | 4种 | D. | 3种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na与水反应 Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向AlCl3溶液中加入过量的NaOH溶液 Al3++3OH-═Al(OH)3↓ | |
| C. | 氢氧化钡溶液与硫酸溶液反应 Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | CO2通入过量澄清石灰水 CO2+Ca2++2OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝:治疗胃酸过多的一种药剂 | |
| B. | 明矾:净水剂 | |
| C. | 烧碱:治疗胃酸过多的一种药剂 | |
| D. | 小苏打:发酵粉主要成分 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5mol | B. | 1.0mol | C. | 1.5mol | D. | 2.0mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
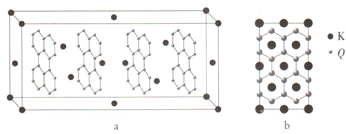 Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子.
Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com