
【题目】有aXn+和bYm-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是
A. b-a=n+m
B. a-b=n-m
C. 核电荷数Y<X
D. 原子半径Y>X
 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:高中化学 来源: 题型:
【题目】随着卤素原子半径的增大,下列递变规律正确的是
A.单质熔、沸点逐渐降低 B.气态氢化物稳定性逐渐增强
C.卤素X-离子的还原性逐渐增强 D.单质的氧化性逐渐增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种烃:①2—甲基丁烷 ②2,2—二甲基丙烷 ③戊烷 ④己烷 ⑤丁
烷,按它们的沸点由高到低的顺序排列正确的是
A. ①>②>③>④>⑤ B. ②>③>⑤>④>①
C. ③>①>②>⑤>④ D. ④>③>①>②>⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将浓度均为0.10mol.L﹣1、体积均为V0L的HX溶液和HY溶液分别加水稀释至体积为VL,其AG[AG=lg ![]() ]随lg
]随lg ![]() 的变化如图所示,下列叙述错误的是( )
的变化如图所示,下列叙述错误的是( ) 
A.HX的酸性强于HY的酸性
B.a点的c(Y﹣)与b点的c(X﹣)相等
C.水的电离程度:a点小于c点
D.若两溶液同时升高温度,则c(Y﹣)和c(X﹣)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤是重要的化工原料,煤的脱硫可减少环境的污染,利用煤矸石中的硫铁矿(主要成分为FeS2)和烟道脱硫得到的硫酸盐生产硫酸的工艺流程如图所示. 
回答下列问题:
(1)硫铁矿和硫酸盐燃烧的装置M的名称为 .
(2)炉气净化过程包括除尘(防止堵塞管道)、洗涤(除去有害物质,防止在转化器中使催化剂中毒)和干燥,干燥的目的是 .
(3)转化器中的催化剂是V2O3 , 而反应条件选择400~500℃和常压的原因是 . 已知每生成1molSO2(g),释放148.5kJ热量,写出该反应的热化学方程式: , 该反应过程中通入稍过量O2的目的是
(4)实验生产中常采用两次转化,其目的是 , 流程中可循环利用的物质是 .
(5)该方法合成硫酸的优点是;按目前技术水平生产硫酸的流程中,反应热的利用约为 ![]() ,试提出利用富余反应热的方法: .
,试提出利用富余反应热的方法: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在蒸馏实验中,下列叙述不正确的是
A.在蒸馏烧瓶中加入约1/3体积的自来水,并放入几粒碎瓷片
B.蒸馏操作中,烧瓶可直接加热
C.冷水从冷凝管的下口入,上口出
D.收集冷凝水时,应弃去开始蒸馏出的部分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示的装置,X、Y都是惰性电极.将电路接通后,向(乙)中滴人酚酞溶液,在Fe极附近显红色.试回答下列问题: 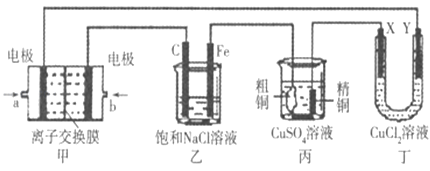
(1)(甲)装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,b处电极上发生的电极反应式是;
(2)如果(丙)装置中精铜电极的质量增加了 6.4g,则乙装置中,铁电极上产生的气体在标准状况下为L,
(3)(丁)装置中Y电极上发生的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( ) 
A.图1某温度下,体积和pH都相同的盐酸和氯化铵溶液加水稀释时的pH 变化曲线,用等浓度NaOH溶液分别和等体积b、c处溶液反应,消耗NaOH溶液体积Vb>Vc
B.图2中曲线a、b分别表示过量纯锌、过量粗锌(含Cu、C杂质)与同浓度等体积盐酸反应过程中产生H2体积的变化趋势
C.图3表示25℃用0.1000 molL﹣1NaOH溶液滴定20.00mL 0.1000 molL﹣1 CH3COOH溶液得到的滴定曲线
D.图4表示某温度下AgBr在水中的沉淀溶解平衡曲线的图象,向AgBr的饱和溶液中加入NaBr固体,可以使溶液由c点到b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2007年度诺贝尔化学奖授予致力于研究氨的合成与催化剂表面积大小关系的德国科学家格哈德埃特尔,以表彰他在“固体表面化学过程”研究中作出的贡献.他研究的氢气与氮气在固体催化剂表面合成氨的反应过程示意图如下: 
(1)图⑤表示生成的NH3离开催化剂表面.则图②和图③的含义分别是、 .
(2)工业上制取硝酸铵的模拟流程图如下: 
请回答下列问题:
(I)此生产过程中,N2与H2合成NH3工业设备名称是;设备中,设置热交换器的目的是;合成氨过程中所用的催化剂是 . 生产中原料气必须进行脱硫处理的目的是 .
(II)在合成硝酸的吸收塔中发生反应的化学方程式是;通入空气的目的是 .
(III)生产硝酸的过程中常会产生一些氮的氧化物,可用如下三种方法处理:
方法一:碱液吸收法:NO+NO2+2NaOH═2NaNO2+H2O;
2NO2+2Na2CO3═NaNO2+NaNO3+CO2
方法二:NH3还原法:8NH3+6NO2 ![]() 7N2+12H2O(NO也有类似的反应)
7N2+12H2O(NO也有类似的反应)
方法三:甲烷吸收法:CH4(g)+2NO2(g)═CO2(g)+N2(g)+2H2O(g)△H=+867kJmol﹣1
(NO也有类似的反应)
上述方法中方法一最大的缺点是;方法三和方法二相比,优点是 , 缺点是 .
(IV)某化肥厂用NH3制备NH4NO3 . 已知:由NH3制NO的产率是94%、NO制HNO3的产率是89%,则制HNO3所用去的NH3的质量占总耗NH3质量(不考虑其它损耗)的%.(保留三位有效数字)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com