
| A. | 二氧化氯是强氧化剂 | B. | 二氧化氯是强还原剂 | ||
| C. | 二氧化氯是电解质 | D. | 二氧化氯分子中氯为-1价 |
分析 ClO2中Cl元素的化合价为+4价,结合信息可知为A级高效安全灭菌消毒剂,与其强氧化性有关,以此来解答.
解答 解:A.二氧化氯中氯的化合价为+4价,化合价为该元素的高价态,所以该物质有较强的氧化性,故A正确;
B.由信息可知,ClO2是强氧化剂,故B错误;
C.ClO2在水溶液或者熔融状态下都不导电,则ClO2不是电解质,故C错误;
D.因为化合物中各元素化合价代数和为零,所以ClO2中氧元素为-2价,故氯元素为+4价,故D错误;
故选A.
点评 本题考查物质的性质,为高频考点,把握习题中的信息及元素的化合价及性质的关系为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 其水溶液显强酸性,俗称石炭酸 | |
| B. | 其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗 | |
| C. | 其在水中的溶解度随温度的升高而增大,超过65℃可以与水以任意比互溶 | |
| D. | 氯化铁溶液中滴入苯酚的水溶液后,溶液呈紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
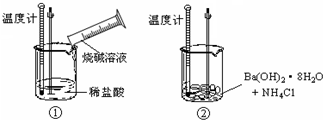
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铝溶液中加入过量的氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| B. | 澄清石灰水与苏打溶液混合:Ca2++OH-+HCO3-=CaCO3↓+H2O | |
| C. | 氯化亚铁溶液中通入氯气:2Fe2++Cl2=2Fe3++2Cl- | |
| D. | 碳酸钙溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
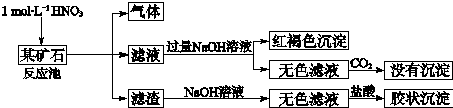
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol | B. | 0.4mol | C. | 0.6mol | D. | 0.8mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com