
X��Y��Z��W���������ڵ�����Ԫ�أ��й����ǵIJ��ֽṹ��������Ϣ���±���ʾ��
| Ԫ�� | ���ֽṹ��Ϣ | ����������Ϣ |
| X | X�ĵ�����˫ԭ�ӷ��ӹ��ɣ���������14������ | X�ж����������XO��XO2��X2O4�ȣ�ͨ�������XO2��X2O4���� |
| Y | Yԭ�ӵĴ�������������������������һ�� | Y���γɶ�����̬�⻯�� |
| Z | Zԭ�ӵ���������������4 | ZԪ�ص���������ϼ���������ϼ۴����͵���6 |
| W | Wԭ�ӵ���������������2n��3(nΪԭ�Ӻ�����Ӳ���) | ��ѧ��Ӧ��Wԭ����ʧȥ���������γ�Wn�� |
�밴Ҫ��ش���������(ע�ⲻ������ĸX��Y��Z��W����)��
(1)X����̬�⻯����ӵĵ���ʽ��________________________��ZԪ�������ڱ��е�λ����________��
(2)X��Y��Z��Ԫ�ص�����������Ӧˮ�����������ǿ������˳����__________________________________________________��
(3)����ʱ��W����������Һ��pH________7(�<������>������)��������__________________________________________________________
_____________________________________________ (�����ӷ���ʽ��ʾ)��
(4)ʵ������X���⻯���ˮ��Һ��ȡW����������ķ�����(�����ӷ���ʽ��ʾ)______________________________________________��
(5)25 �桢101 kPaʱ��32 g Y����ͼ���̬�⻯����ȫȼ�������ȶ���������ʱ�ų�1 780.6 kJ��������д���÷�Ӧ���Ȼ�ѧ����ʽ��_______
______________________________________________________________��
�������������Ƴ�XΪNԪ�أ�YΪCԪ�أ�ZΪClԪ�أ���Wԭ�ӵ���������������2n��3(nΪԭ�Ӻ�����Ӳ���)�һ�ѧ��Ӧ��Wԭ����ʧȥ���������γ�Wn������2n��3��n��n��3����WΪAlԪ�ء�
�𰸡�(1)  ���������ڢ�A��
���������ڢ�A��
(2)HClO4>HNO3>H2CO3
(3)<��Al3����3H2OAl(OH)3��3H��
(4)Al3����3NH3·H2O===Al(OH)3����3NH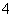
(5)CH4(g)��2O2(g)===CO2(g)��2H2O(l)
��H����890.3 kJ/mol


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪��
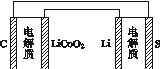
����ӵ�ص��ܷ�ӦΪ
LixC��Li1��xCoO2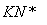 C��LiCoO2
C��LiCoO2
����ص��ܷ�Ӧ2Li��S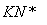 Li2S
Li2S
�й��������ֵ��˵����ȷ����(����)
A������ӵ�طŵ�ʱ�� Li����Ǩ��
B������س��ʱ��﮵缫������ԭ��Ӧ
C�����������ֵ�صı�������ͬ
D����ͼ��ʾ������ӵ�ظ�����س��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��������Ҫ���л�����ԭ�ϣ�������ϩ����ֱ��ˮ�Ϸ�����ˮ�Ϸ��������ش��������⣺
��1�����ˮ�Ϸ���ָ�ֽ���ϩ��Ũ���ᷴӦ����������������C2H5O SO3H������ˮ�������Ҵ���д����Ӧ��Ӧ�Ļ�ѧ����ʽ__________________________________��
SO3H������ˮ�������Ҵ���д����Ӧ��Ӧ�Ļ�ѧ����ʽ__________________________________��
��2����֪��
�״���ˮ��Ӧ 2CH3OH(g)==CH3OCH3(g)+ H2O (g) 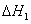 =
=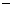 23.9 KJ﹒mol-1
23.9 KJ﹒mol-1
�״���ϩ����Ӧ 2CH3OH(g)== C2H4(g)+ 2H2O (g) 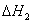 =
=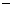 29.1 KJ﹒mol-1
29.1 KJ﹒mol-1
�Ҵ��칹����Ӧ C2H5OH (g) ==CH3OCH3(g)
(g) ==CH3OCH3(g) 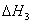 =+50.7KJ﹒mol-1
=+50.7KJ﹒mol-1
����ϩ����ֱ��ˮ�Ϸ�ӦC2H4(g)+H2O(g)==C2H5OH(g)��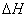 =______KJ﹒mol-1������ˮ�Ϸ���ȣ�����ֱ��ˮ�Ϸ����ŵ���____________________________________��
=______KJ﹒mol-1������ˮ�Ϸ���ȣ�����ֱ��ˮ�Ϸ����ŵ���____________________________________��
��3����ͼΪ����ֱ��ˮ�Ϸ���ϩ��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ������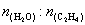 =1:1��
=1:1��
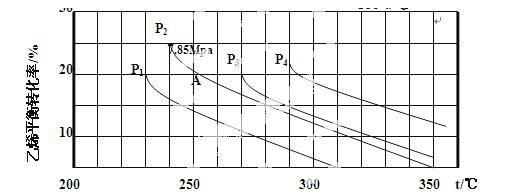
����ʽ������ϩˮ�����Ҵ���Ӧ��ͼ��A���ƽ�ⳣ��Kp=_______����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�����������
��ͼ��ѹǿ��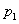 ��
��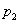 ��
��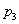 ��
��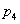 ���Ĵ�С˳��Ϊ_________��������_________��
���Ĵ�С˳��Ϊ_________��������_________��
������ֱ��ˮ�Ϸ������õĹ�������Ϊ������/������Ϊ��������Ӧ�¶�290�棬ѹǿ6.9MPa��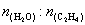 =0.6:1����ϩ��ת����Ϊ5%����Ҫ��һ�����ת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ��_________��_________��
=0.6:1����ϩ��ת����Ϊ5%����Ҫ��һ�����ת���ʣ����˿����ʵ��ı䷴Ӧ�¶Ⱥ�ѹǿ�⣬�����Բ�ȡ�Ĵ�ʩ��_________��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����(����)
A�����ԣ�H2CO3<C6H5OH<CH3COOH
B�����ԣ�Ba(OH)2<Ca(OH)2<KOH
C���۵㣺MgBr2<SiCl4<BN D���е㣺PH3<NH3<H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
X��Y��Z��W��R���ֶ����ڷǽ�������Ԫ����Ԫ�����ڱ��е�λ����ͼ��ʾ�������й�˵����ȷ����(����)
| X | Y | ||
| Z | W | R |
A.Zλ�ڵ������ڢ�A��
B��X��Y����̬�⻯����ȶ��ԣ�X>Y
C��ԭ�Ӱ뾶��С˳��Z>W>Y
D��W��R������������Ӧˮ��������ԣ�W>R
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NaBH4 (BԪ�صĻ��ϼ�Ϊ+3)��H2O2Ϊԭ�ϵĵ�أ�������ΪͨѶ���ǵĸ��ܵ�ء���缫��������ΪPt��C����������ΪMnO2������ԭ����ͼ��ʾ������˵����
��ȷ����( )
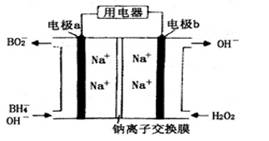
A���õ�ع���ʱNa+��a��������b����
B���缫b��ԭ��ص�����
C���õ�صĸ�����ӦΪ��BH4��+8OH����8 e��= BO2��+6H2O
D����·��ͨ��6.02��1022������ʱ������������H2O20.1mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�����Ũ�ȹ�ϵ�������У���ȷ���ǣ� ��
A��25��ʱ����0.1mol��L��1NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�
c(Na��)��c(NH4+)��c(SO42��)��c(OH��)��c(H��)
B��25��ʱ��NaB��Һ��pH��8��c(Na��) + c(B��)��9.9��10��7mol��L��1
C��0.1 mol��L��1��NaHCO3��Һ�У�c(OH��)��c(CO32��)��c(H+)��c(H2CO3)
D��ͬ���£�pH��ͬʱ����Һ���ʵ���Ũ�ȣ�c(CH3COONa)<c(NaHCO3)<c(C6H5ONa)<c(Na2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ƥा�������������Ч����Ƥ�ؾ��п������˾���Ч��������һ�������¿ɷ���ת������ͼ��ʾ���й�˵����ȷ����( )
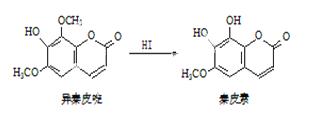
A������Ƥ�����Ƥ�ػ�Ϊͬϵ��
B������Ƥष���ʽΪC11H12O5
C����Ƥ��һ���������ܷ����ӳɷ�Ӧ����ȥ��Ӧ��ȡ����Ӧ
D��1mol��Ƥ��������2molBr2(Ũ��ˮ�е�)��4molNaOH��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ܱ������У������з�Ӧ��
N2(g)+3H2(g) 2NH3(g) ��H=-93.4 kJ��mol-1
2NH3(g) ��H=-93.4 kJ��mol-1
�йظ÷�Ӧ��������ȷ���ǣ� ��
A.����������и��ɷֵ�Ũ�Ȳ��ٱ仯����÷�Ӧ�Ѵ�ƽ��״̬
B.��1 mol N2��3 mol H2��ַ�Ӧ�ﵽƽ��ʱ���ų�����������93.4 kJ
C.���������̸÷�Ӧ�ﵽƽ�������ʱ�䣬�Ӷ����N2��ת����
D.��С�����������v(��)����v(��)��С��ƽ�������ƶ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com