
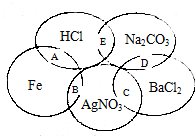
 ��ͼΪһ��Ԫ��ͼ����С����ͼ��������д���������ʣ�ͼ���ཻ���������ʾ��ɷ�����ѧ��Ӧ��A��B��C��D��E��ʾ����Ӧ�Ļ�ѧ��Ӧ����ش��������⣺
��ͼΪһ��Ԫ��ͼ����С����ͼ��������д���������ʣ�ͼ���ཻ���������ʾ��ɷ�����ѧ��Ӧ��A��B��C��D��E��ʾ����Ӧ�Ļ�ѧ��Ӧ����ش��������⣺���� ��1����Ӧ�д���Ԫ�ػ��ϼ۵ı仯�ķ�ӦΪ������ԭ��Ӧ��������Ԫ�ػ��ϼ۵ı仯�ķ�ӦΪ��������ԭ��Ӧ��
��2������������ԭ��Ӧ���������������Դ�������������������жϣ�
��3��A��ӦΪFe��HCl��Ӧ�����Ȼ�����������������ȡ������ӦA�����Һ���þƾ���С�ļ����������Ȼ�������������FeCl3������������ԭ��Ӧ��FeCl3�ڷ�ˮ��ˮ�����ɽ��壮
��� �⣺��1��A��ӦΪFe��HCl��Ӧ��Fe��HԪ�صĻ��ϼ۷����仯������������ԭ��Ӧ��
B��ӦΪFe�����������û���Ӧ��Fe��AgԪ�صĻ��ϼ۷����仯������������ԭ��Ӧ��
C��ӦΪ�Ȼ�����������֮��ĸ��ֽⷴӦ������������ԭ��Ӧ��
D��ӦΪ�Ȼ�����̼����֮��ĸ��ֽⷴӦ������������ԭ��Ӧ��
E��ӦΪHCl��̼����֮��ĸ��ֽⷴӦ������������ԭ��Ӧ��
�������ڷ�������ԭ��Ӧ����CDE��
�ʴ�Ϊ��CDE��
��2�������˳�����Ag����H�ĺ��棬�������ԣ�Ag+��H+��Fe��HCl��Ӧ�����������Ȼ��������������ԣ�H+��Fe2+�����������ԣ�Ag+��H+��Fe2+��
�ʴ�Ϊ��Ag+��H+��Fe2+��
��3��A��ӦΪFe��HCl��Ӧ�����Ȼ�����������������ȡ������ӦA�����Һ���þƾ���С�ļ����������Ȼ�������������FeCl3������������ԭ��Ӧ��FeCl3�ڷ�ˮ��ˮ�����ɽ��壬�÷�ӦΪFeCl3+3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3HCl��
�ʴ�Ϊ��FeCl3+3H2O$\frac{\underline{\;\;��\;\;}}{\;}$Fe��OH��3�����壩+3HCl���У�
���� ���⿼��������ԭ��Ӧ��������ѧ���ķ��������Ŀ��飬ע�����������ԭ��Ӧ����������Ԫ�ػ��ϼ۵ĽǶ���ʶ��ظ�������ʵ����ʣ��ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SiO2��CaCO3��������������������� | |
| B�� | NaCl��Һ��NaOH������������������ | |
| C�� | Na2O2��ĩ��Na2O������������������м��� | |
| D�� | FeSO4��Һ[Fe2��SO4��3]������������NaOH��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
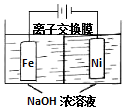 ���й㷺��;��Na2FeO4���õ�ⷨ��ȡ��Fe+2H2O+2OH-$\frac{\underline{\;ͨ��\;}}{\;}$FeO42-+3H2�����乤��ԭ����ͼ��ʾ������������ȷ���ǣ�������
���й㷺��;��Na2FeO4���õ�ⷨ��ȡ��Fe+2H2O+2OH-$\frac{\underline{\;ͨ��\;}}{\;}$FeO42-+3H2�����乤��ԭ����ͼ��ʾ������������ȷ���ǣ�������| A�� | ���һ��ʱ��������ҵ�c��OH-������ | |
| B�� | Na+������������������ | |
| C�� | ������Ӧʽ��2H2O+2e-=H2��+2OH- | |
| D�� | �������У�������1 mol OH-ʱ��ͬʱ����33.6 L H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 3mol C+1mol D | |
| B�� | 1mol A+0.5mol B+1.5mol C+0.5mol D | |
| C�� | 1mol A+0.5mol B+1.5mol C | |
| D�� | 4mol A+2mol B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6.72L | B�� | 4.48L | C�� | 2.24L | D�� | 1.12L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
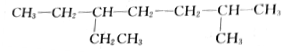 ��������2-��-5-�һ�����
��������2-��-5-�һ�����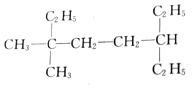 ��������3��3-����-6-�һ�����
��������3��3-����-6-�һ����� ��������2-��-3��6-���һ�����
��������2-��-3��6-���һ����� ��������2��4��4��5-�ļ����飮
��������2��4��4��5-�ļ����飮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���ͻ���� | |
| A | ��ɫ�Լ�ƿ�е�Ũ������ֻ�ɫ | ����ȶ����ֽ�����NO2���ܽ������� |
| B | �ڲ������ܿڵ�ȼ����������ʻ�ɫ | ����ȼ�� |
| C | ij��ɫ��Һ�еμ���ˮ�����Ȼ�̼�������ã��²������ɫ | ��Һ�к��е����� |
| D | ��CuSO4��Һ��ͨ��H2S���к�ɫ�������� | �����ܵ�CuS���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
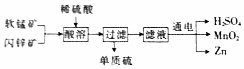 ��ҵ�Ͽ������̿���Ҫ�ɷ�MnO2������п����Ҫ�ɷ�ΪZnS���Ʊ��ɵ���������MnO2��Zn���乤��������ͼ��ʾ������˵���д�����ǣ�������
��ҵ�Ͽ������̿���Ҫ�ɷ�MnO2������п����Ҫ�ɷ�ΪZnS���Ʊ��ɵ���������MnO2��Zn���乤��������ͼ��ʾ������˵���д�����ǣ�������| A�� | ������������Ԫ�صļ�̬û�б仯 | |
| B�� | ���������е������ѭ������ | |
| C�� | ͨ������У�����Zn����ʱ������ԭ��Ӧ | |
| D�� | ͨ������У������ĵ缫��ӦʽΪMn2+-2e-+2H2O�TMnO2+4H+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com