
在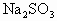 溶液中加硫酸可制得
溶液中加硫酸可制得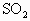 ,试写出该反应的离子方程式:________;产生的
,试写出该反应的离子方程式:________;产生的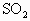 通入饱和石灰水中有白色沉淀产生,试写出该反应的离子反应式:________.
通入饱和石灰水中有白色沉淀产生,试写出该反应的离子反应式:________.
科目:高中化学 来源: 题型:
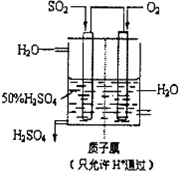 (2010?聊城模拟)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
(2010?聊城模拟)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.| 1 |
| 2 |
| 10 |
| 3 |
c(C
| ||
c(S
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广西省高三8月月考理综试卷(解析版) 题型:选择题
下列实验操作正确的是
A.可用氨水除去试管内壁上的银镜
B.硅酸钠溶液应保存在带玻璃塞的试剂瓶中
C.将三氯化铁溶液蒸干,可制得无水三氯化铁
D.锌与稀硫酸反应时,要加大反应速率可滴加少量硫酸铜
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com