
【题目】某化工厂生产化工原料的同时会产生多右种废液,其有机废液的主要成分为苯胺、苯酚、苯甲醇(都微溶于水),其无机废液的主要污染成分为Cr2O72-,该工厂处理废液的方法如下:
I.利用物质的酸碱性,从有机废液中分离、回收有机物
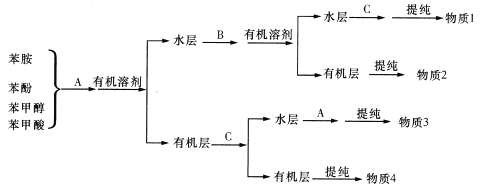
(1)物质A为______,物质B为______, 物质C为_________。(填写化学式)
(2)若想选用一种试剂仅仅将苯甲酸与其他种物质分开,则应选用的试剂是______。
II.利用纳米级Cu2O处理含有Cr2O72-的酸性废水
已知:Cu2O![]() Cu+CuSO4;pH=5时Cr3+会形成Cr(OH)3沉淀
Cu+CuSO4;pH=5时Cr3+会形成Cr(OH)3沉淀
(3)工业上用肼(N2H4)与新制的Cu(OH)2反应制备纳米级Cu2O,同时放出N2,该反应的化学方程式为____________。
(4)光照时,会在形成的微电极上发生电极反应,反应原理如下图所示,

对Cu2O的作用提出两种假设:
a. Cu2O作光催化剂;
b. Cu2O与Cr2O72-发生氧化还原反应
己知:Cu2O的添加量是1.74×10-4mol/L,Cr2O72-的初始浓度是9.60×10-4mol/L;对比实验,反应1.5小时结果如右图所示。结合试剂用量数据和实验结果可得到的结论是假设_____成立,写出该过程的正极反应方程式:_______________。
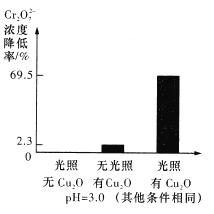
(5)溶液的pH对Cr2O72-降解率的影响如下图所示。

由上图可知,pH=3时,Cr2O72-的降解率最大;pH=2与pH=5时,Cr2O72-的降解率低的原因分别可能是___________、______________。
【答案】 NaOH或Na2CO3 CO2 HCl NaHCO3溶液 N2H4+4Cu(OH)2=2Cu2O+N2↑+6H2O a Cr2O72-+14H++6e-=2Cr3++7H2O pH=2时,Cu2O会转化为Cu和Cu2+ pH=5时,会产生Cr(OH)3沉淀覆盖在催化利Cu2O表面,影响反应继续进行
【解析】苯胺、苯酚、苯甲醇都微溶于水,而苯甲酸与苯酚加入氢氧化钠或碳酸钠溶液,转化为可溶性物质,加入有机溶剂萃取苯胺和苯甲醇,分液得到水层和有机层。水层中含有苯酚钠和苯甲酸钠,苯酚的酸性弱于碳酸,苯甲酸的酸性强于碳酸,因此通入CO2即可把苯酚钠转化为苯酚,物质2是苯酚。盐酸是强酸,向苯甲酸钠溶液中加入盐酸生成苯甲酸,即物质1是苯甲酸;苯胺含有氨基,能与盐酸反应转化为可溶性物质,分液得到水层,加入氢氧化钠再转化为苯胺,物质3是苯胺,物质4是苯甲醇。
(1)根据以上分析可知物质A为NaOH或Na2CO3,物质B为CO2,物质C为HCl。(2)若想选用一种试剂仅仅将苯甲酸与其他种物质分开,由于其余物质与碳酸氢钠均不反应,则应选用的试剂是NaHCO3溶液。(3)工业上用肼(N2H4)与新制的Cu(OH)2反应制备纳米级Cu2O,同时放出N2,根据原子守恒和电子得失守恒可知该反应的化学方程式为N2H4+4Cu(OH)2=2Cu2O+N2↑+6H2O。(4)若发生氧化还原反应,则存在比例:3Cu2O~Cr2O72-,计算9.60×10-4×3×69.5%=2.00×10-3>1.74×10-4mol/L;实验可以看到只有氧化亚铜和只有光照时,Cr2O72-的转化率很低,说明反应条件是光照条件下和Cu2O同时存在,因此假设a成立,正极发生得到电子的还原反应,则正极反应式为Cr2O72-+14H++6e-=2Cr3++7H2O;(5)由图可知:pH=2.5时Cu2O会歧化(转化)为Cu 和Cu2+;根据已知信息可知pH=5时,会产生Cr(OH)3沉淀覆盖在催化剂Cu2O表面,影响反应继续进行。


科目:高中化学 来源: 题型:
【题目】通过用水溶解、过滤、蒸发等操作,可将下列各组混合物分离的是( )
A.硝酸钾、氢氧化钠
B.氧化铜、二氧化锰
C.氯化钾、二氧化锰
D.硫酸铜、氢氧化钡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】多晶硅是单质硅的一种形态,是制造硅抛光片、太阳能电池及高纯硅制晶的主要原料。已知多晶硅第三代工业制取流程如图所示:
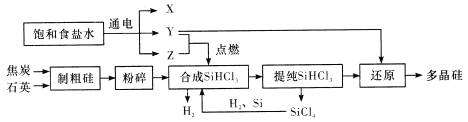
下列说法错误的是
A. Y、Z分别为H2、Cl2
B. 制取粗硅的过程中焦炭与石英会发生副反应生成碳化硅,在该副反应中,氧化剂与还原剂的物质的量之比为1:1
C. SiHCl3极易水解,其完全水解的产物为H2SiO3、H2、HCl,据此推测SiHCl3中硅元素的化合价为+2价
D. Y与SiHCl3制备多晶硅的反应属于置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在2 L密闭容器内,反应2NO2(g)![]() N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
N2O4(g) ΔH=-180 kJ·mol-1,n(NO2)随时间变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO2)/mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
(1)用NO2表示0~2 s内该反应的平均速度___________.在第5 s时,NO2的转化率为_____。根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是_____________________。
(2)上述反应在第3 s后达到平衡,能说明该反应已达到平衡状态的是______。
a.单位时间内,消耗2 mol NO2的同时生成1 mol的N2O4
b.容器内压强保持不变
c.v逆(NO2)=2v正(N2O4)
d.容器内密度保持不变
(3)在2 s内,该反应_______(“吸收”或“放出”) _______热量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质组成、分类正确的是( )
A.盐酸、硫酸、硝酸都是强氧化性酸
B.新制氯水、氨水的溶质分别是次氯酸、氨分子
C.纯碱、烧碱的成分分别是碳酸钠、氢氧化钠
D.苯、聚苯乙烯、聚乙烯的组成元素以及元素质量比相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据电解质在溶液中的电离情况,我们划分出了酸、碱、盐,通过学习我们知道酸和碱都有通性,而盐是没有通性的,其本质原因是( )
A.盐不能电离出阳离子
B.盐不能电离出阴离子
C.盐不能电离出H+或OH﹣
D.盐不能电离出共同的离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,几种难溶氢氧化物的饱和溶液中金属离子浓度的负对数与溶液的pH关系如下图所示。下列说法正确的是
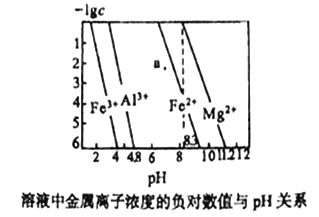
A. a点代表Fe(OH)2饱和溶液
B. Ksp[Fe(OH)3]< Ksp[Al(OH)3]< Ksp[Fe(OH)2]< Ksp[Mg(OH)2]
C. 向0.1mol/L Al3+、Mg2+、Fe2+混合溶液中,逐滴滴加稀NaOH溶液,Mg2+最先沉淀
D. 在pH=7的溶液中,Fe3+、Al3+、Fe2+能大量共存
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,有关说法不正确的是( )
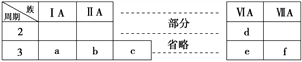
A. 元素b的单质不能与酸性氧化物发生化学反应
B. a、b、d、f四种元素的离子半径:f>d>a>b
C. 元素c的氧化物既能与酸反应又能与碱反应
D. a、c、e的最高价氧化物对应的水化物之间能够相互反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com