
用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)H2SO4溶解Al2O3的离子方程式是____________________________________。
(2)将MnO4-氧化Fe2+的离子方程式补充完整:
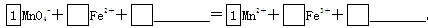
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度为0.1 mol·L-1
根据表中数据解释步骤Ⅱ的目的:________。
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2。
① 向 Ⅲ 的沉淀中加入浓HCl并加热,能说明沉淀中存在MnO2的现象是__________。
② Ⅳ 中加入MnSO4的目的是_____________________________________________。
(1)Al2O3+6H+=2Al3++3H2O
(2)5 8H+ 5 4H2O
(3)pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)①生成黄绿色气体 ②除去过量的MnO4-
【解析】本题主要考查化工制备知识,意在考查考生的信息挖掘能力、实验探究能力以及解答综合实验问题的能力。由题给条件,加入过量稀硫酸,发生反应:Al2O3+3H2SO4=Al2(SO4)3+3H2O,FeO·xFe2O3+(3x+1)H2SO4=FeSO4+xFe2(SO4)3+(3x+1)H2O,过滤后得到的滤液为Al2(SO4)3、FeSO4、Fe2(SO4)3和硫酸的混合溶液,滤渣为SiO2;向滤液中加入过量的高锰酸钾溶液,目的是将Fe2+全部氧化为Fe3+,然后调节pH约为3,由题给表格(生成氢氧化物沉淀的pH)信息知,此时Fe3+全部转化为氢氧化铁沉淀,上层溶液为KMnO4和硫酸铝,根据题给信息,一定条件下,MnO4-可与Mn2+反应生成MnO2,从而把上层溶液中的MnO除去,最后浓缩、结晶、分离。得到产品。(1)H2SO4溶解Al2O3的离子方程式是Al2O3+6H+=2Al3++3H2O。(2)由题意,在酸性条件下高锰酸钾把Fe2+氧化成Fe3+,所以反应物中添上H+,生成物中添上H2O,配平得:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O。(3)步骤Ⅱ的目的是将Fe2+全部氧化为Fe3+,然后调节pH约为3,使Fe3+全部转化为Fe(OH)3沉淀。(4)①根据反应:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O可知,有黄绿色气体产生时说明沉淀中有MnO2;②加入MnSO4可除去过量的MnO4-。
MnCl2+Cl2↑+2H2O可知,有黄绿色气体产生时说明沉淀中有MnO2;②加入MnSO4可除去过量的MnO4-。


科目:高中化学 来源: 题型:
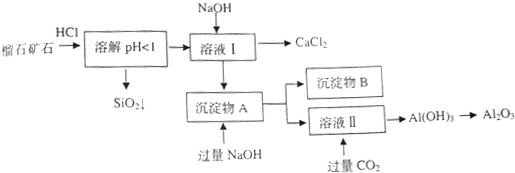
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 12.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 1 |
| 2 |
| 3 |
| 2 |
 2CO2的平衡常数为K1;反应4Fe+3O2
2CO2的平衡常数为K1;反应4Fe+3O2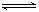 2Fe2O3的平衡常数K2,则反应3CO+Fe2O3
2Fe2O3的平衡常数K2,则反应3CO+Fe2O3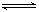 2Fe+3CO2的平衡常数K与K1、K2的关系式
2Fe+3CO2的平衡常数K与K1、K2的关系式
|
|
| ||
| ||
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
| n(C) |
| n(Fe2O3) |
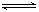 HSO3-+OH-
HSO3-+OH-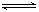 HSO3-+OH-
HSO3-+OH-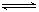 2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是
2AlCl3(g)+3CO(g)△H>0,欲提高金属铝的氯化效果,不可采取的措施是查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| 高温高压 |
| ||
| 高温高压 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 TiCl4(l)+O2 (g);△H=+151kJ/mol反应难于发生,所以工业上不能直接由TiO2和Cl2反应来制取TiCl4.当反应体系中加入碳后,反应分如下两步进行(如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热相同).
TiCl4(l)+O2 (g);△H=+151kJ/mol反应难于发生,所以工业上不能直接由TiO2和Cl2反应来制取TiCl4.当反应体系中加入碳后,反应分如下两步进行(如果一个反应可以分几步进行,则各分步反应的反应热之和与该反应一步完成时的反应热相同). TiCl4 (l)+2CO (g);△H=
TiCl4 (l)+2CO (g);△H= TiCl4(l)+O2 (g)顺利进行的原因是
TiCl4(l)+O2 (g)顺利进行的原因是
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 1 |
| 2 |
| 3 |
| 2 |
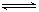
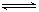
| ||
| ||
| n(C) |
| n(Fe2O3) |
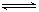
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com