
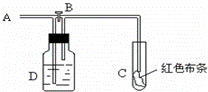
如图:A处通入氯气.关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色.由此作出的判断正确的是( )
A. D中不可能是浓硫酸 B. 通入的氯气含有水蒸气
C. D中不可能是NaOH溶液 D. D中可以是饱和食盐水
考点: 氯气的化学性质.
专题: 卤族元素.
分析: 由图可知,关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色,则A为潮湿的氯气,D中的液体可干燥或吸收氯气,以此来解答.
解答: 解:由图可知,关闭B阀时,C处红色布条无变化,打开B阀时,C处红色布条褪色,则A为潮湿的氯气,D中的液体可干燥或吸收氯气,
A.D中可以为浓硫酸,干燥氯气,符合题意,故A错误;
B.由上述分析可知,通入的氯气含有水蒸气,故B正确;
C.D中的液体可能为NaOH溶液,吸收氯气,符合题意,故C错误;
D.D中液体不能为饱和食盐水,若为食盐水,则关闭B阀时,C处红色布条褪色,故D错误;
故选B.
点评: 本题考查氯气的性质,为高频考点,侧重学生分析与推断能力的考查,注意HClO具有漂白性,把握开关闭合观察到的不同现象确定A的成分及D中的液体为解答的关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
铁及其化合物在生产和生活中有着广泛的应用.
(1)氧化铁是重要工业颜料,用废铁屑制备它的流程如下:
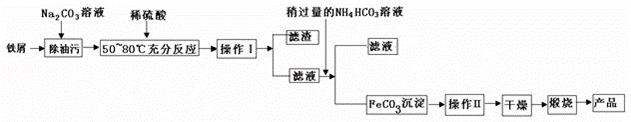
回答下列问题:
①操作Ⅰ、Ⅱ的名称分别是 、 .
②写出在空气中煅烧FeCO3的化学方程式 ;
③煅烧如果不充分,产品中将有Fe2+存在,试设计实验检验产品中有无Fe2+.
(2)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定.
a.称取2.850g绿矾(FeSO4•7H2O)产品,溶解,在250mL容量瓶中定容;
b.量取25.00mL待测溶液于锥形瓶中;
c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.
①写出酸性KMnO4溶液与FeSO4溶液反应的离子方程式
②计算上述样品中FeSO4•7H2O的质量分数为 已知M(FeSO4•7H2O)=278g/mol]
③滴定达到终点时锥形瓶中溶液颜色变化为
④下列操作会导致样品中FeSO4•7H2O的质量分数的测定结果偏高的有 .
a.未干燥锥形瓶
b.盛装标准液的滴定管没有用标准液润洗
c. 滴定终点时滴定管尖嘴中产生气泡
d.量取待测液,视线注视刻度时开始平视、结束俯视.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于药品保存方法不正确的是( )
A. 二氧化硅不与强酸反应,可用石英器皿盛放氢氟酸
B. 硅酸钠溶液应保存在带橡胶塞的试瓶中
C. 液溴易挥发,在存放溴的试剂瓶中应加水封
D. 浓硝酸存放在带有玻璃塞的棕色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
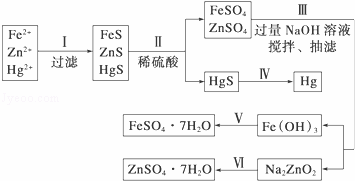
某工厂排出的污水中含有大量的Fe3+、Zn2+、Hg2+三种金属离子.以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4•7H2O)和汞的方案.
NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉
如图
(1)步骤Ⅱ所发生反应的离子方程 .
步骤Ⅲ中抽滤的目的是 ,该步骤产生Fe(OH)3的反应的离子方程式为 .
(3)步骤Ⅵ中得到硫酸锌溶液的离子方程式为 .
(4)欲实现步骤Ⅴ,需加入的试剂有 、 ,所涉及的主要操作依次为 .
(5)步骤Ⅳ常用的方法是 ,该步骤是否对环境有影响? (填“是”或“否”),如有影响,请你设计一个绿色环保方案来实现步骤Ⅳ的反应: .
(6)该研究小组的同学在强碱溶液中,用次氯酸钠与Fe(OH)3反应获得了高效净水剂Na2FeO4,该反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 摩尔是物质的数量单位,含有6.02×1023个微粒的物质叫做1摩尔
B. 1mol氧含有6.02×1023个氧原子
C. 在标准状况下,任何物质的摩尔体积约为22.4L/mol
D. 一定质量的气体的体积随压强增大和温度降低而变小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是()
A. 为了提高生活用水的卫生标准,自来水厂常同时使用Cl2和FeSO4•7H2O进行消毒、净化,以改善水质
B. 铝表面有一层致密的氧化薄膜,故铝制容器可用来腌制咸菜等
C. 
从分类的角度看,混合物、分散系、胶体的从属关系如图所示:
D. 借助扫描隧道显微镜,应用STM技术可实现对原子或分子的操纵
查看答案和解析>>
科目:高中化学 来源: 题型:
可溶性钡盐有毒,医院中常用硫酸钡这种钡盐作为内服造影剂。医院抢救钡离子中毒患者时,除催吐外,还需要向中毒者胃中灌入硫酸钠溶液。已知:某温度下,Ksp(BaCO3)=5.1×10-9 mol2 • L-2;Ksp(BaSO4)= l.1×10-10 mol2 • L-2 下列推断正确的是
A.不用碳酸钡作为内服造影剂,是因为Ksp(BaCO3)>Ksp(BaSO4)
B.抢救钡离子中毒患者时,若没有硫酸钠,可以用碳酸钠溶液代替
C.若误饮c(Ba2+)= 1.0 ×10-5 mol • L﹣1的溶液时,会引起钡离子中毒
D.可以用0.36 mol • L﹣1的Na2SO4溶液给钡离子中毒患者洗胃
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W为四种短周期主族元素,其中X、Z同族,Y、Z同周期,W是短周期主族元素中原子半径最大的,X原子最外层电子数是核外电子层数的3倍,Y的最高正价与最低负价代数和为6.下列说法正确的是( )
|
| A. | Y元素最高价氧化物对应的水化物化学式H2YO4 |
|
| B. | 原子半径由小到大的顺序为:X<Z<Y |
|
| C. | Y、Z两种元素气态氢化物中,Z的气态氢化物最稳定 |
|
| D. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com