
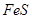 与一定浓度的
与一定浓度的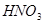 反应,生成
反应,生成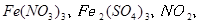
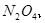
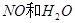 ,当
,当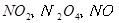 的物质的量之比为
的物质的量之比为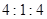 时,实际参加反应的
时,实际参加反应的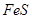 与
与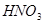 的物质的量之比为( )。
的物质的量之比为( )。
| A.1:6 | B.2:15 | C.2:3 | D.16:25 |
A
解析试题分析: 令参加反应的FeS为1mol,则溶液中Fe2(SO4)3为1/3mol,Fe(NO3)3为1/3mol,反应中Fe元素、S元素化合价升高,N元素化合价降低,令NO2、N2O4、NO的物质的量分别为4amol、amol、4amol,根据电子转移守恒有:1×(3-2)+1×[6-(-2)]=4a×(5-4)+a×(5-4)×2+4a×(5-2),解得a=0.5,故NO2、N2O4、NO的物质的量分别为2mol、0.5mol、2mol,故起氧化剂作用的HNO3为2mol+0.5mol×2+2mol=5mol,起酸的作用的硝酸生成Fe(NO3)3,故起酸的作用的硝酸为1/3mol×3=1mol,参加反应的硝酸为5mol+1mol=6mol,故实际参加反应的FeS与HNO3的物质的量之比为1mol:6mol=1:6,故选A。
考点:本题考查了氧化还原反应有关计算,难度中等,利用电子转移守恒与元素守恒计算是关键,转移守恒思想在氧化还原反应计算中的运用。


 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案科目:高中化学 来源: 题型:单选题
对于反应:TiCl4+4Na=4NaCl+Ti,下列说法正确的是
| A.该反应说明钠是强还原剂,可用于冶炼金属 |
| B.该反应条件是TiCl4在熔融状态或水溶液中 |
| C.Ti是氧化剂 |
| D.TiCl4是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有一未完成的离子方程式____+XO3-+6H+=3X2+3H2O,据此判断,氧化产物和还原产物的物质的量之比为
| A.1∶1 | B.3∶1 | C.5∶1 | D.7∶1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4 mol/L和2 mol/L,取10 mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下的气体的体积为(设反应中HNO3被还原成NO) ( )
| A.0.448 L | B.0.672 L | C.0.896 L | D.0.224 L |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是 ( )
| A.KClO3是氧化剂 |
| B.发生氧化反应与还原反应的氯元素的质量比为5:1 |
| C.H2SO4既不是氧化剂又不是还原剂 |
| D.1mol KClO3参加反应时有10mol电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应能说明卤素非金属性活泼顺序是Cl>Br>I的是
①2HClO4+Br2(气) = 2HBrO4+Cl2
②2NaBr+Cl2= 2NaCl+Br2
③2KI+Cl2= 2KCl+I2
④2KI+Br2= 2KBr+I2
| A.①②③ | B.①②④ | C.②③④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知:Cu+2Fe3+=Cu2++2Fe2+;Zn+2Fe3+=2Fe2++Zn2+。现将等物质的量的CuSO4、FeCl3和Zn于水中充分反应,所得混合物中除了SO42—、Cl—外,还含有( )
| A.Zn2+、Fe3+、Cu | B.Cu2+、Fe3+、Zn |
| C.Zn2+、Cu2+、Fe2+、Fe | D.Zn2+、Fe2+、Cu2+、Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知I2+SO32—+H2O==2I—+SO42—+2H+。某无色溶液中可能含有I-、NH4+、Cu2+、SO32-,向该溶液中加入少量溴水,溶液仍呈无色,则下列关于溶液的判断正确的是
①肯定不含I- ②肯定不含Cu2+ ③肯定含有SO32- ④可能含有I-
| A.②③④ | B.①②③ | C.①③ | D.①② |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
黑火药爆炸时发生:S+2KNO3+3C=K2S+N2↑+3CO2↑,其中被还原的物质是( )
| A.S和KNO3 | B.C 和S | C.KNO3 | D.C 和KNO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com