
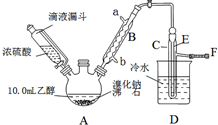
 实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H2SO4(浓)+NaBr$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr↑.CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O.有关数据见表:
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H2SO4(浓)+NaBr$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HBr↑.CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O.有关数据见表:| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红色液体 |
| 密度/(g•cm-3) | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
分析 (1)根据装置图可知A仪器的名称;
(2)滴液漏斗可以使漏斗的上方和下方的压强相等,使浓磷酸顺利流下;
(3)在温度过高或浓硫酸的浓度过大的情况下,浓硫酸与溴化氢发生氧化还原反应生成溴和二氧化硫,会使收集到的粗产品呈橙色;
(4)给A加热可以加快反应速率蒸出溴乙烷;实验中产生的二氧化硫、溴化氢、溴等可以用稀NaOH溶液吸收;
(5)通过E的末端插入水面以下冷却减少溴乙烷的挥发;
(6)根据溴乙烷和溴的性质,逐一分析能够和溴化氢反应且不能和溴乙烷反应试剂,注意除杂不能引进新的杂质;
(7)①溴乙烷的密度大于水,所以分液都是从分液漏斗的下口放出;
②10mL乙醇的质量为0.79×10g=7.9g,其物质的量为0.172mol,所以理论制得溴乙烷的物质的量为0.172mol,其质量为18.75g,根据产率=$\frac{实际产量}{理论产量}$×100%计算.
解答 解:(1)根据装置图可知A仪器的名称为三颈烧瓶,
故答案为:三颈烧瓶;
(2)滴液漏斗可以使漏斗的上方和下方的压强相等,使浓磷酸顺利流下,而分液漏斗没有这个功能,
故答案为:平衡压强,使浓硫酸顺利流下;
(3)在温度过高或浓硫酸的浓度过大的情况下,浓硫酸与溴化氢发生氧化还原反应生成溴和二氧化硫,会使收集到的粗产品呈橙色,反应方程式为2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2↑+SO2↑+2H2O,
故答案为:2HBr+H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$Br2↑+SO2↑+2H2O;
(4)加热的目的是加快反应速率,温度高于38.4°C溴乙烷全部挥发蒸馏出来,实验中产生的二氧化硫、溴化氢、溴等会污染空气,所以可以用稀NaOH溶液吸收;
故答案为:升高温度加快反应速率,同时使生成的溴乙烷气化分离出来促进平衡移动;吸收SO2、Br2、HBr防止空气污染;
(5)导管E的末端须在水面以下,通过冷却得到溴乙烷,减少溴乙烷的挥发,提高产率;
故答案为:使溴乙烷充分冷凝,提高产率;
(6)A.氢氧化钠,加氢氧化钠会引起溴乙烷水解,故A错误;
B.除去溴乙烷中的少量杂质Br2,加碘化钾会引入碘单质杂质 故B错误;
C.加亚硫酸钠只与溴反应不与溴乙烷反应,故c正确;
D.碳酸氢钠溶液呈碱性,和溴单质、溴乙烷反应,故D错误;
故选C;
(7)①溴乙烷的密度大于水,所以分液都是从分液漏斗的下口放出,
故答案为:下口;
②10mL乙醇的质量为0.79×10g=7.9g,其物质的量为0.172mol,所以理论制得溴乙烷的物质的量为0.172mol,其质量为18.75g,所以溴乙烷的产率=$\frac{10.0g}{18.75g}$×100%=53.3%,
故答案为:53.3%.
点评 本题考查有机物制备实验,涉及实验室HBr的制备、物质的分离提纯、对操作与原理的分析评价等,综合考查学生实验分析的能力、知识迁移运用能力,题目难度中等.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:解答题
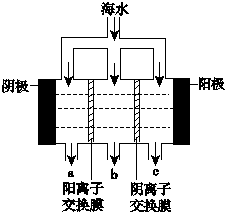 《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.
《科学》曾评出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一种重要的自然资源,是人类赖以生存不可缺少的物质.水质优劣直接影响人体健康.海洋是化学资源宝库,海洋资源的综合利用具有广阔的前景.人类把海水淡化,就可以得到大量的饮用水,常规蒸馏法,技术和工艺比较完备,但也存在较大缺陷,大量推广离子交换法和电渗析法.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量NaHCO3、Na2CO3分别与同浓度盐酸完全反应,消耗的盐酸体积Na2CO3是NaHCO3的二倍 | |
| B. | Na2O2和Na2O均可以和盐酸反应生成相应的盐,都属于碱性氧化物 | |
| C. | 将澄清石灰水分别加入NaHCO3和Na2CO3两种盐溶液中,只有Na2CO3溶液产生沉淀 | |
| D. | Na2O2和Na2O中Na2O更稳当,Na2O2在一定条件下可以转化为Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 药品 | 制取气体 | 量气管中的液体 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固体、浓氨水 | NH3 | |
| Ⅲ | 镁铝合金、足量NaOH溶液 | H2 | H2O |
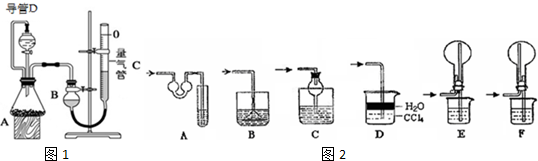
| 编号 | 镁铝合金质量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 376.6mL |
| ② | 1.0g | 10.0mL | 364.7mL |
| ③ | 1.0g | 10.0mL | 377.0mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸一般要保存棕色试剂瓶中,置于阴凉处,原因是:4HNO3$\frac{\underline{\;见光或受热\;}}{\;}$2NO2↑+O2↑+2H2O | |
| B. | 配制240ml浓度为1 mol•L-1的NaOH溶液,需将NaOH固体放在烧杯中,用托盘天平称取10.00g,选用250ml的容量瓶进行配制 | |
| C. | 常温下可用铁质或铝制容器储运浓硝酸,是因为常温下二者不发生反应 | |
| D. | 铵盐在加热时都会分解产生氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 39g苯中含有C═C键数为1.5NA | |
| B. | 0.5molFeBr2与标准状况下33.6L氯气反应时转移电子数为3NA | |
| C. | 1L0.5mol•L-1的NaClO溶液中含有的ClO-离子数为0.5NA | |
| D. | 常温常压下,14g由C2H4和C3H6组成的混合气体中含有的原子总数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com