
| A. | 氯气的水溶液可以导电,说明氯气是电解质 | |
| B. | 漂白粉和明矾都常用于自来水的处理,二者的作用原理是相同的 | |
| C. | 氯气可以使湿润的有色布条褪色,但实际起漂白作用的物质是次氯酸而不是氯气 | |
| D. | 氯水中加入红色鲜花,红花褪色,说明溶液中有Cl2存在 |
分析 A、水溶液中或熔融状态导电的化合物为电解质分析判断;
B、漂白粉利用强氧化性消毒杀菌,明矾石利用铝离子水解生成的氢氧化铝胶体具有吸附杂质作用净水;
C、氯气无漂白性,起漂白性的是次氯酸;
D、氯水中含有次氯酸,具有漂白性,所以向氯水中加入有色布条一会儿红花褪色,不能说明溶液中有Cl2存在.
解答 解:A、电解质必须是化合物,氯气是单质,故A错误;
B、漂白粉是利用强氧化性消毒,而明矾净水是利用Al3+水解生成的Al(OH)3胶体吸附杂质,二者的作用原理是不相同,故B错误;
C、氯气可以使湿润的有色布条褪色,是因为Cl2+H2O=HClO+HCl,次氯酸具有漂白作用,氯气无漂白性,故C正确;
D、氯水中含有次氯酸,具有漂白性,所以向氯水中加入有色布条一会儿红花褪色,不能说明溶液中有Cl2存在,故D错误;
故选C.
点评 本题考查了氯气的性质分析判断,注意漂白性的物质判断,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 铅笔芯的主要原料是石墨,儿童使用时不会引起中毒 | |
| B. | CO有毒,生有煤炉的居室可放置数盆清水,能有效地吸收CO,防止煤气中毒 | |
| C. | “汽水”浇灌植物有一定的道理,其中CO2的释放,有利于植物的光合作用 | |
| D. | 硅的提纯与应用,促进了半导体元件与集成芯片业的发展,可以说“硅是信息技术革命的催化剂” |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
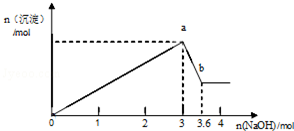 现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图.
现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
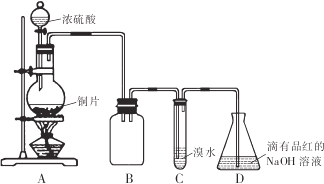
| 序号 | 实 验操作 | 现 象 | 结 论 |
| ① | 加几小块CaCO3固体 | 有气泡产生 | I或Ⅱ |
| ② | 滴加少量淀粉KI溶液,振荡 | Ⅲ | |
| ③ | 滴加少量溴水,振荡 | Ⅱ | |
| ④ | 滴加少量酸性KMn04溶液、振荡 | 溶液为紫色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 异常情况 | 可能原因分析 |
| A | 萃取:液体静置不分层 | 加入萃取剂的量较多 |
| B | 分液:分液漏斗中的液体难以滴下 | 没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
| C | 蒸馏:温度计读数达到了馏分的沸点且历时10分钟,锥形瓶中却无液体 | 温度计位置错误,或装置漏气,或冷凝水方向反了 |
| D | 检验Fe2+:加入KSCN溶液,溶液呈红色 | Fe2+已部分被氧化成Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6.75 g | B. | 4.05g | C. | 2.70 g | D. | 1.80 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.5g甲基所含有的电子数是NA | |
| B. | 28g乙烯所含共用电子对数目为6NA | |
| C. | 17g羟基所含有的电子数是10NA | |
| D. | 标准状况下,2.24 LCCl4中含Cl原子数目等于0.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
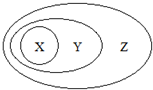 如图用交叉分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
如图用交叉分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )| X | Y | Z | |
| A | CuSO4•5H2O | 盐 | 纯净物 |
| B | 胶体 | 分散系 | 混合物 |
| C | 碱性氧化物 | 氧化物 | 化合物 |
| D | 置换反应 | 氧化还原反应 | 离子反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
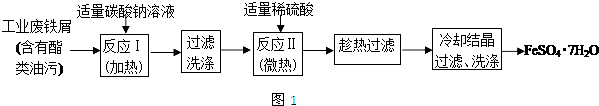

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com