
芳香类化合物C8H8O2能与NaHCO3溶液反应生成CO2,该芳香化合物连在碳原子上的氢原子被氯原子取代后的一氯代物共有(不含立体异构)( )
A. 15种 B. 16种 C. 17种 D. 18种
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
下列试剂的保存或使用正确的是
A. 实验室的氯水需要保存在棕色试剂瓶中
B. 漂白粉比氯水稳定,可露置在空气中
C. 称量氢氧化钠固体时,可在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码
D. 金属钠可保存在煤油、四氯化碳等有机溶剂中
查看答案和解析>>
科目:高中化学 来源:2017届山东省泰安市高三第一轮复习质量检测(一模)理科综合化学试卷(解析版) 题型:填空题
乙炔是重要的化工原料,广泛用于有机合成和氧炔焊等。生产乙炔的方法有多种,如电石法、甲烷裂解法等。
(1)在Co(NO3)2催化下,乙炔可被50%的浓硝酸(硝酸被还原为NO2)在20~70℃时直接氧化为H2C2O4·2H2O。
①该反应的化学方程式为________________________;
②实际生产中硝酸可循环利用而不被消耗,用方程式说明:___________________。
(2)电石法原理为:由石油焦与生石灰在电炉中生成电石CaC2(含Ca3P2、CaS等杂质), 电石与水反应生成C2H4(含PH3及H2S等杂质)。
①已知焦炭固体与氧化钙固体每生成l g CaC2固体,同时生成CO气体吸收7.25kJ的 热量,则该反应的热化学方程式为_____________________________________;
②用CuSO4溶液净化乙炔气体,去除PH3的反应之一为:4CuSO4+PH3+4H2O===4Cu↓+H3PO4+4H2SO4,每去除1 mol PH3,该反应中转移电子的物质的量为__________;
③反应H2S(aq)+Cu2+(aq)===CuS(s)+2H+(aq)的平衡常数为________________;(已知Ksp(CuS)=1.25×10-36,H2S的Kal=1×10-7,Ka2=1×10-13)
④电石法工艺流程简单、容易操作、乙炔纯度高,缺点是_______(举1例)。
(3)甲烷裂解法原理为:2CH4(g) C2H2(g)+3H2(g)△H,实验测得该反应的Kp(用平衡分压代替浓度计算的平衡常数,分压=总压×物质的量分数)与温度的关系如图所示:
C2H2(g)+3H2(g)△H,实验测得该反应的Kp(用平衡分压代替浓度计算的平衡常数,分压=总压×物质的量分数)与温度的关系如图所示:
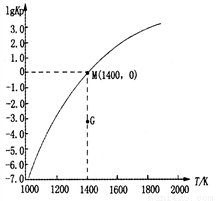
①该反应的△H________0(填“>”、“=”或“<”);
②图中G点v(正)______v(逆)(填“>”、“=”或“<”);
③M点时,若容器中气体的总物质的量为1 mol,则总压P与n(CH4)、n(C2H2)及n(H2)之间的关系为_________。
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三下学期第二次质量监测理综化学试卷(解析版) 题型:简答题
工业上常以铬铁矿(主要成分为亚铬酸亚铁FeCr2O4,还含有Al2O3、SiO2等杂质)为主要原料生产红矾钠(Na2Cr2O7),某实验小组模拟其流程如下图所示:
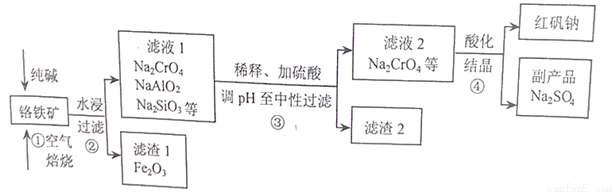
(1)FeCr2O4中Cr的化合价为____________,步骤①焙烧时所用的仪器名称为_________;步骤①中生成Na2CrO4的化学方程式为________________________。
(2)步骤①煅烧反应极慢,需要升温至纯碱呈熔融状态,反应速率才加快,其主要原因为________。
(3)步骤②过滤时所用到的玻璃仪器有________________;
(4)涉骤③用硫酸将溶液的pH调至中性,所得滤渣2的主要成分是__________、__________;
(5)步骤④向滤液2加入硫酸酸化过程中,溶液由黄色变为橙色,反应的离子方程式为___________。
(6)下图是Na2Cr2O7·2H2O和Na2SO4的溶解度曲线,步骤④中获得副产品Na2SO4的实验操作方法为____________________。
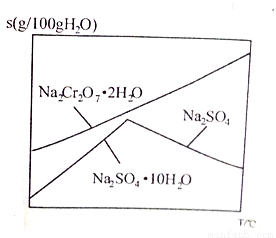
查看答案和解析>>
科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:实验题
氮化铝(AlN)是一种新型无机非金属材料。为了分析某AlN样品(样品中的杂质不与NaOH溶液反应)中 AlN的含量,某实验小组设计了如下两种实验方案。已知:AlN+NaOH+H2O=NaAlO2+NH3↑
【方案1】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
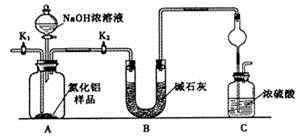
(1)上图装置中,U形管B中所装固体为________,C中球形干燥管的作用是_______________________。
(2)关闭K1打开K2,再打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是_______________________________________。
(3)由于上述装置还存在____________缺陷,导致测定结果偏高。
【方案2】按以下步骤测定样品中AlN的纯度:
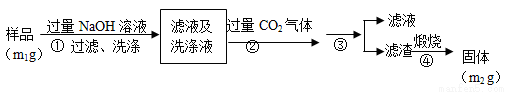
(4)步骤②生成沉淀的离子方程式为___________________。
(5)步骤③的操作中用到的主要玻璃仪器是_________。AlN的纯度是__________(用m1、m2表示)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:选择题
下列溶液中微粒的物质的量浓度关系正确的是
A. 室温下,向0.01mol/LNH4HSO4溶液中滴加Na0H溶液至中性:c(Na+)>c(SO42-)>c(NH4+)> c(OH-)= c(H+)
B. Na2CO3溶液:c(Na+)+ c(H+)=c(HCO3-)+c(CO32-)+ c(OH-)
C. 等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)= c(HCO3-)+c(H2CO3)
D. 氯水中:2c(Cl2)=c(ClO-)+c(Cl-)+c(HClO)
查看答案和解析>>
科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:选择题
中国古代化学成绩斐然,下列说法错误的是
A. 古代造纸是以木材等为原料,用去除杂质后的纤维素制成的,纤维素属子天然高分子
B. 火药是由硫磺、木炭、硝酸钾按照一定比例混合制得的
C. “China”来源于闻名于世的我国陶瓷,陶瓷是一种硅酸盐产品
D. 司母戊鼎是商朝铸造的青铜器,它是由纯铜制作的
查看答案和解析>>
科目:高中化学 来源:2017届河南省安阳市高三第二次模拟考试理综化学试卷(解析版) 题型:简答题
一种带有多孔结构的镍铝合金对H2具有较强的吸附性,其高催化活性和热稳定性使得该镍铝合金被用于很多工业过程中和有机合成反应中。下图是以镍黄铁矿(主要成分为NiS、FeS等)为原料制备该镍铝合金的工艺流程图:
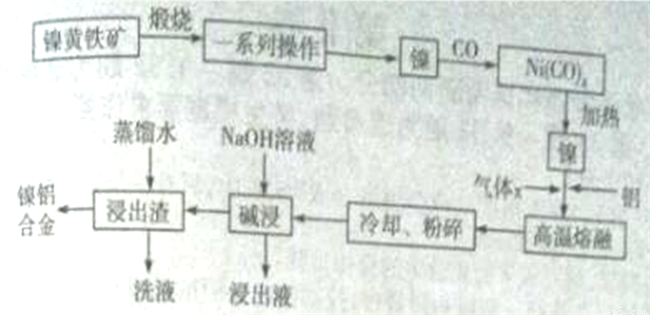
回答下列问题:
(1)Ni(CO)4中C、O化合价与CO中的C、O化合价相同,则Ni化合价为_______价。
(2)在空气中“煅烧”生成Ni2O3和Fe2O3,写出Fe2O3的化学方程式________________。
(3)操作“镍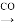 Ni(CO)4
Ni(CO)4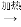 镍”的目的是__________。
镍”的目的是__________。
(4) Ni、Al高温熔融时,气体x的作用是___________。对“高温熔融”物冷却后,需要进行粉碎处理,粉碎处理的目的是________________。
(5)“碱浸”可以使镍产生多孔结构,从而增强对H2的吸附性,“浸出液”中的主要离子是_____________;“浸出液”中的铝元素可循环利用,写出回收“浸出液”中的铝元素,并制备“高温熔融”时的原料Al的流程:_____________(示例:CuO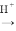 Cu2+
Cu2+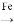 Cu)。
Cu)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com