
【题目】下列与有机物结构、性质相关的叙述中,正确的是( )
A.煤中含有大量苯等芳香烃,煤是芳香烃的主要来源
B.肥皂可以通过高分子化合物油脂发生皂化反应制得
C.鸡蛋清中加入CuSO4溶液会产生盐析现象,析出的蛋白质可再溶于水
D.煤油是石油的分馏产品,可用于保存少量金属钠
科目:高中化学 来源: 题型:
【题目】已知 2Fe3+ +2I- =2Fe2+ +I2,2Fe2+ +Cl2 =2Fe3+ +2Cl-,则有关离子的还原性由强到弱的顺序为()
A.Cl->Fe2+>I-B.Fe2+>I->Cl-C.I->Fe2+>Cl-D.Fe2+>Cl->I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水.请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)___________。
(2)④、⑤、⑥、⑦四种溶液中NH![]() 浓度由大到小的顺序是(填序号)_______________。
浓度由大到小的顺序是(填序号)_______________。
(3)将③和④按体积比1∶2混合后,混合液中各离子浓度由大到小的顺序是:__________________。
(4)已知t ℃时,KW=1×10-13,则t ℃(填“>”、“<”或“=”)________25℃。在t ℃时将pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烷烃的结构简式为

(1)用系统命名法命名该烃:______________________________________。
(2)若该烷烃是由烯烃加氢得到的,则原烯烃的结构有___________种。(不包括立体异构,下同)
(3)若该烷烃是由炔烃加氢得到的,则原炔烃的结构有____________ 种。
(4)该烷烃在光照条件下与氯气反应,生成的一氯代烷最多有_______ 种。
(5)写出由甲苯制取TNT的反应方程式______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C、P、Cl、Fe等元素及其化合物有重要的应用,回答下列问题:
(1)C原子的价电子轨道表达式为__________________ 。
(2)CC14分子的空间构型是______________,其中心原子采取______________杂化,与CC14互为等电子体的一种离子是__________________ (填写离子符号)。
(3)PC13属于________________分子(填“极性”或“非极性”)。
(4)FeO、NiO的晶体结构均与NaCl晶体结构相同,其中Fe2+与Ni2+的离子半径分别为 7.8×l0-2nm、6.9×l0-2nm,则熔点 FeO_________NiO (填 “>”、“ <”或“=”),原因是___________________。
(5)已知FeCl3的沸点:319℃,熔点:306℃,则FeCl3的晶体类型为______________。
(6)已知Fe单质有如图所示的两种常见堆积方式:
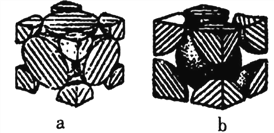
其中属于体心立方密堆积的是___________(填“a”或“b”);若单质Fe按a方式紧密堆积,原子半径为rpm,NA表示阿伏加德罗常数的值,则单质Fe的密度为________g·cm-3 (列出算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中用KClO3在MnO2催化下受热分解制取氧气;从反应后的KCl和MnO2的混合物中分离、回收这两种物质。
(1)写出KClO3在MnO2催化下受热分解制取氧气的化学方程式:____________________;
(2)从KCl和MnO2的混合物中分离、回收这两种物质的实验方案如下:
![]()
步骤②的名称为______________,MnO2固体的洗涤方法______________________;
(3)步骤③的名称为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.有机物的结构可用“键线式”简化表示.CH3-CH=CH-CH3可简写为![]() .有机物X的键线式为:
.有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式_______________;
(2)Y在一定条件下发生聚合反应,写出其反应的化学方程式_______________________;
(3)二甲苯苯环上的一溴代物有6种同分异构体,这些一溴代物与生成它们的对应二甲苯的熔点分别为:
一溴代二甲苯 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205℃ |
对应二甲苯 | 13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |
由以上数据推断:
熔点为234℃的一溴代二甲苯的结构简式为____________;熔点为-27℃的二甲苯的名称为____________;
II.治疗甲型H1N1流感的常见药物有奥司他韦、扎那米韦、金刚乙胺及金刚烷胺以及预防药物如中药材金银花、大青叶等。其中金刚烷胺可按下列路线合成:

已知狄尔斯阿德耳反应(也称双烯合成反应)如下所示:

试回答下列问题:
(1)B的结构式为________________(填键线式)。
(2)上述物质中,属于同分异构体的是________(填字母)。
(3)上述反应中,属于加成反应的是________(填数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。
下面是它的一种实验室合成路线:
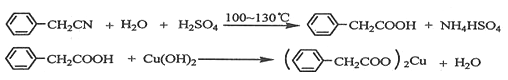
制备苯乙酸的装置示意图如右(加热和夹持装置等略):
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____________________________。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中仪器c的作用是_______________________。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是___________________。下列仪器中可用于分离苯乙酸粗品的是_______________。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(3)提纯粗苯乙酸的方法是__________________________________________。
(4)将苯乙酸加入到乙醇与水的混合溶剂中充分溶解后,加入Cu(OH)2搅拌30min,过滤。滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com