
【题目】用H2消除酸性废水中的NO2-是一种常 用的电化学方法。其反应原理如图所示,下列说法不正确的是( )
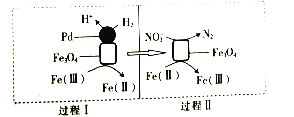
A.Fe3O4在该反应中作催化剂
B.Pd上发生的反应为H2-2e-═2H+
C.总反应为3H2+2NO2-═N2+2OH-+2H2O
D.Fe(Ⅱ)与Fe(Ⅲ)之间相互转化起到了传递电子的作用
【答案】C
【解析】
过程Ⅰ中,负极H2-2e-=2H+,正极2Fe3++2e-=2Fe2+;过程Ⅱ中,负极6Fe2+-6e-=6Fe3+,正极2NO2-+6e-+8H+=N2+4H2O。调整电子守恒,将电极反应式相加,即可得到3H2+2NO2-+2H+![]() N2+4H2O,由此进行解答。
N2+4H2O,由此进行解答。
A. 由以上分析可知,Fe3O4先消耗后生成,在反应中起催化剂作用,A正确;
B. 由过程Ⅰ中的转化关系,可得出Pd上发生的反应为H2-2e-═2H+,B正确;
C. 电解质溶液提供H+,总反应为3H2+2NO2-+2H+![]() N2+4H2O,C不正确;
N2+4H2O,C不正确;
D. Fe(Ⅱ)和Fe(Ⅲ)通过得失电子发生相互转化,实际上起到传递电子作用,D正确。
故选C。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.35Cl与37Cl互为同素异形体
B.O2与O3互为同位素
C.![]() 与CH3CH2CH2CH3互为同分异构体
与CH3CH2CH2CH3互为同分异构体
D.乙烯与CH3—C≡CH互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的电子排布式为_________________。
(2)实验室用KSCN溶液、苯酚(![]() )检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
(3)FeCl3的熔点为306℃,沸点为315℃。FeCl3的晶体类型是________。FeSO4常作补铁剂,SO42-的立体构型是__________。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1 mol Fe(CO)5分子中含________molσ键,与CO互为等电子体的离子是__________(填化学式,写一种)。
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为_____。

(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-的最短核间距为___________pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃分子的球棍模型(如图),据此回答下列问题:

(1)等质量的上述烃燃烧耗氧量最高的是(填对应字母)__;
(2)属于同系物的是(填对应字母)___;
(3)所有原子都在同一平面上的是(填对应字母)___;
(4)一卤代物总类最多的是(填对应字母)___;
(5)实验室制D的化学方程式___;
(6)写出G合成烈性炸药(TNT)的化学方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国科技大学改进Pd/Al2O3催化H2还原CO2制备甲醇的生产工艺,其机理如图所示,下列说法不正确的是( )
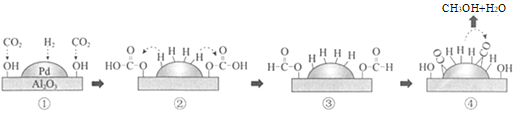
A.金属钯是优良的贮氢材料
B.①→②为CO2发生加成反应
C.④中CO被氧化为CH3OH
D.生成甲醇的总反应方程式是CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成 ![]() (部分试剂和反应条件已去).
(部分试剂和反应条件已去).

请回答下列问题:
(1)A的名称为__________。
(2)分别写出 B、F 的结构简式:B_____、F_____。
(3)反应①~⑦中属于消去反应的是_____,属于加成反应的是_____(填代号)。
(4)根据反应![]() +Br2
+Br2![]() ,写出在同样条件下CH2=CH—CH=CH2 与等物质的量Br2反应的化学方程式:__________________。
,写出在同样条件下CH2=CH—CH=CH2 与等物质的量Br2反应的化学方程式:__________________。
(5)写出第④步的化学方程式_______________。
(6)下列有机物分子中,在核磁共振氢谱图中能给出三种峰(信号)且强度之比为 1∶1∶2 的是_______________。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酰氯(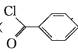 )是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
)是制备染料,香料药品和树脂的重要中间体,以光气法制备苯甲酰氯的原理如下(该反应为放热反应):
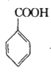 +COCl2
+COCl2![]()
![]() +CO2+HCl
+CO2+HCl
已知物质性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 溶解性 |
苯甲酸 | 122.1 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
碳酰氯(COCl2) | -188 | 8.2 | 较易溶于苯、甲苯等。遇水迅速水解,生成氯化氢,与氨很快反应,主要生成尿素[CO(NH2)2]和氯化铵等无毒物质 |
苯甲酰氯 | -1 | 197 | 溶于乙醚、氯仿和苯。遇水或乙醇逐渐分解,生成苯甲酸或苯甲酸乙酯和氯化氢 |
三氯甲烷(CHCl3) | -63.5 | 63.1 | 不溶于水,溶于醇、苯。极易挥发,稳定性差,450℃以上发生热分解 |
I.制备碳酰氯
反应原理:2 CHCl3+O2![]() 2HCl+COCl2
2HCl+COCl2
甲. 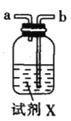 乙.
乙. 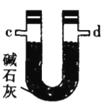 丙.
丙. 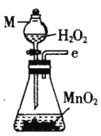 丁.
丁.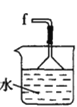 戊.
戊. 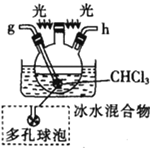
(1)仪器M的名称是____________
(2)按气流由左至右的顺序为___________→c→d→_________→_________→_________→_________→_________.
(3)试剂X是_______________(填名称)。
(4)装置乙中碱石灰的作用是____________。
(5)装置戊中冰水混合物的作用是____________;多孔球泡的作用是________________。
Ⅱ.制备苯甲酰氯(部分夹持装置省略)

(6)碳酰氯也可以用浓氨水吸收,写出该反应的化学方程式:______________。
若向三颈烧瓶中加入610g苯甲酸,先加热至140~150℃,再通入COCl2,充分反应后,最后产品经减压蒸馏得到562g苯甲酰氯,则苯甲酸的转化率为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空
(1)水存在如下平衡:H2O![]() H++OH-,保持温度不变向水中加入NaHSO4固体,水的电离平衡向___(填“左”或“右”)移动,,所得溶液显__性,Kw__(填“增大”“减小”或“不变”)。
H++OH-,保持温度不变向水中加入NaHSO4固体,水的电离平衡向___(填“左”或“右”)移动,,所得溶液显__性,Kw__(填“增大”“减小”或“不变”)。
(2)常温下,0.1mol·L-1CH3COONa溶液的pH为9,则由水电离出的c(H+)=___。
(3)若取pH、体积均相等的NaOH溶液和氨水分别加水稀释m倍、n倍后pH仍相等,则m___n(填“>”“<”或“=”)。
(4)已知HA和HB均为弱酸,且酸性HA>HB,则等浓度的NaA和NaB溶液中,PH大小关系为NaA___NaB(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物莫沙朵林(F)是一-种镇痛药,它的合成路线如下:
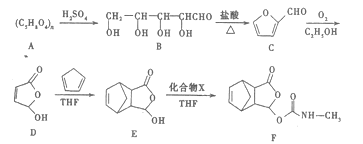
(1)A![]() B的转化属于______________反应(填反应类型),1mol B与足量的金属钠反应可以生成标况下的氢气_________L,B的沸点远高于相对分子质量接近的烃类,其原因是_______。
B的转化属于______________反应(填反应类型),1mol B与足量的金属钠反应可以生成标况下的氢气_________L,B的沸点远高于相对分子质量接近的烃类,其原因是_______。
(2)化合物D中含氧官能团的名称为__________
(3)化合物C与新制氢氧化铜悬浊液反应的化学方程式为____________
(4)下列有关化合物E的说法中正确的是__________(填序号)。
A.化合物E的分子式为C9H12O3
B.化合物E能使酸性KMnO4溶液和溴水褪色
C.1mol E发生加成反应最多消耗2 mol H2
D.E中既有非极性共价键也有极性共价键
(5)写出同时满足下列条件的E的一种同分异构体的结构简式:__________;
I.分子的核磁共振氢谱图中有4组峰;
Ⅱ.能发生银镜反应和水解反应;
Ⅲ.能与FeCl3溶液发生显色反应,且与溴水反应。
1mol该同分异构体与足量NaOH溶液反应,最多可消耗________molNaOH。
(6)已知E+X![]() F为加成反应,则化合物X的结构简式为__________。
F为加成反应,则化合物X的结构简式为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com