
 有关苏糖的说法不正确的是( )
有关苏糖的说法不正确的是( )| A. | 苏糖能发生银镜反应 | |
| B. | 苏糖属于单糖 | |
| C. | 苏糖在一定条件下,能发生加成和取代反应 | |
| D. | 苏糖与葡萄糖互为同分异构体 |
科目:高中化学 来源: 题型:填空题
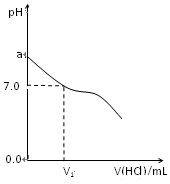 常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸.溶液的PH值的变化关系如图所示.
常温下,在20.0mL 0.20mol/LCH3COONa溶液中滴加0.20mol/L的稀盐酸.溶液的PH值的变化关系如图所示. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇、乙酸均能与 Na 反应放出 H2,二者分子中官能团相同 | |
| B. | 乙烯和苯都能与 H2 发生加成反应,说明二者均含有碳碳双键 | |
| C. | 苯可以在空气中燃烧,但不能被酸性高锰酸钾溶液氧化 | |
| D. | 乙醇在铜催化作用下,能发生还原反应生成乙醛 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气的性质很活泼,它与氢气混合后立即发生爆炸 | |
| B. | 可以用氢氧化钙溶液吸收实验室制取氯气时多余的氯气 | |
| C. | 检验Cl2中是否混有HCl方法是将气体通入硝酸银溶液 | |
| D. | 除去Cl2中的HCl气体,可将气体通入饱和食盐水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 步骤①,最好用硫酸来溶解烧渣 | |
| B. | 步骤②,涉及的离子反应为FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+ | |
| C. | 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾 | |
| D. | 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:实验题
如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
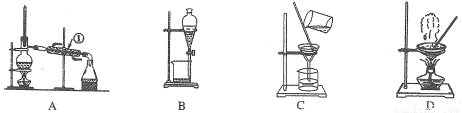
(1)从氯化钾溶液中得 到氯化钾固体,选择装置 (填代表装置图的字母,下同);除去自来水中的C1?等杂质,选择装置 。
到氯化钾固体,选择装置 (填代表装置图的字母,下同);除去自来水中的C1?等杂质,选择装置 。
(2)从碘水中分离出I2,选择装置 ,该分离方法的名 称为 。
称为 。
(3)装置A中①的名称是 ,进水的方向是从 口进水。装置B在分液时为使液体顺利滴下,除打开上口活塞外,还应进行的具体操作是 。
(4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:

粗盐中含Ca2+、Mg2+、SO42-等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④加入略过量的盐酸 ⑤溶解 ⑥过 滤 ⑦蒸发
滤 ⑦蒸发
正确的操作顺序是 (填写序号)。
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
(5)用化学方程式回答加入Na2CO3溶液的作用:_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  蒸馏水 | B. | 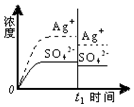 0.010mol•L-1 Ag2SO4溶液 | ||
| C. | 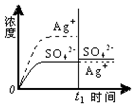 0.020mol•L-1 Na2SO4溶液 | D. | 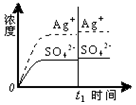 0.040mol•L-1 AgNO3溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com