
| A、用稀硝酸清洗做过银镜反应的试管 |
| B、用稀盐酸清洗做高锰酸钾分解实验的试管 |
| C、用氢氧化钠溶液清洗盛过硅酸的试管 |
| D、用四氯化碳清洗做过碘升华的烧杯 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
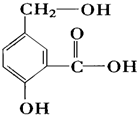 (1)用工业酒精制造的假酒中通常含有
(1)用工业酒精制造的假酒中通常含有查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1 |
| B、0.125mol?L-1 |
| C、0.2 mol?L-1. |
| D、0.25mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
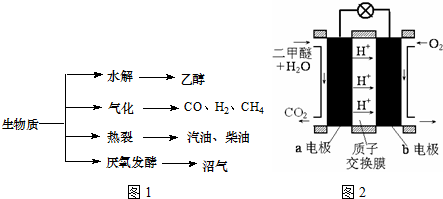
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 放出Q1 kJ | 吸收Q2 kJ | 放出Q3 kJ |
| 反应物转化率 | α 1 | α 2 | α 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com