
下列离子组能大量共存的是
A.Na+ Ag+ OH- Cl- B.Na+ Mg2+ SO42- NO3-
C.K+ NH4+ CO32- OH- D.H+ Fe2+ ClO- NO3-
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源: 题型:
《化学与生活》
化学与社会经济建设、生态文明建设、人类健康保障等密切相关。
(1)(5分)材料是经济和生态文明建设的重要物质基础。
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是 ▲ 。
②橡胶是制造轮胎的重要原料,橡胶属于 ▲ (填字母)。
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生 ▲ 腐蚀。发生该腐蚀时的负极反应式为 ▲ 。
(2)(5分)防治环境污染,改善生态环境已成为全球共识。
①2013年,全国多个省市出现严重的雾霾天气。导致雾霾形成的主要污染物是 ▲ (填字母);
A.O2 B.CO2 C.PM2.5
②采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾.
A.废电池 B.易拉罐 C.玻璃瓶
在焚烧处理前,除废电池外,还有 ▲ (填字母)应剔除并回收,随意丢弃电池造成的主要危害是 ▲ 。
③漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学反应方程式是 ▲ 。
(3)(5分)保证食品安全、保持营养均衡,是保障人体健康的基础。
①维生素C能促进人体生长发育。下列富含维生素C的是 ▲ (填字母)。
A.牛肉 B.辣椒 C.鸡蛋
②缺乏某种微量元素将导致甲状腺肿大,且造成智力损害,该微量元素是 ▲
A.碘 B.铁 C.钙
③人体内蛋白质在蛋白酶作用下,水解为 ▲ ,在鸡蛋清溶液中加入饱和硫酸铵溶液有沉淀析出的过程称为 ▲ 。
④使用青霉素可能会产生过敏,在用药前患者一定要进行 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面各装置图能达到实验目的的是
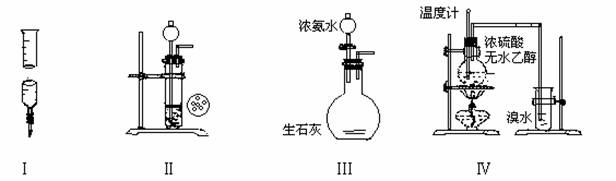
A.实验Ⅰ量取20.0mL的H2SO4待测液放入锥形瓶中
B.实验Ⅱ用CaC2和饱和食盐水反应制取C2H2
C.实验Ⅲ制取氨气
D.实验Ⅳ溴水褪色证明了乙烯可以与溴发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
加碘食盐中含有的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解。在酸性条件下碘酸钾是一种较强的氧化剂,可与碘化物、亚硫酸盐等还原性物质反应。工业生产碘酸钾的流程如下:

(1)步骤②中氢氧化钾的主要作用是 ▲ 。
(2)参照下表碘酸钾的溶解度,操作③得到碘酸钾晶体,可经过 ▲ 、过滤、洗涤、干燥等步骤。
| 温度/℃ | 20 | 40 | 60 | 80 |
| KIO3/100g水 | 8.08 | 12.6 | 18.3 | 24.8 |
(3)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O; I2+2S2O32-=2I-+S4O62-
为了测定加碘食盐中碘的含量,某学生设计了如下实验:准确称取wg食盐,加适量蒸馏水使其完全溶解;再用稀硫酸酸化所得溶液,加入过量KI溶液,使KIO3与KI反应完全;最后加入指示剂,以物质的量浓度为2.00×10-3mol·L-1的Na2S2O3溶液滴定,消耗10.00mL时恰好反应完全。
① 在滴定过程中,所用的玻璃仪器为 ▲ 、 ▲ 。
② 该实验可以用 ▲ 作指示剂,滴定终点的现象是 ▲ 。
③ 下列有关该滴定实验的说法不正确的是 ▲ 。
A.滴定管在使用前必须检查是否漏水并润洗
B.滴定时眼睛注视滴定管内溶液液面变化
C.为减小实验误差,可用少量的蒸馏水冲洗锥形瓶内壁
D.终点读数时俯视会导致碘的含量偏低
④加碘食盐样品中的碘元素含量是 ▲ g·kg-1(以含w的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组中的性质比较,正确的是
①酸性:HClO4>HBrO4>HIO4 ②碱性:KOH>Ca(OH)2>Mg(OH)2
③稳定性:HCl>H2S>PH3 ④原子半径:Na<Mg<Al
A.①②④ B.②③④ C.①②③ D.全部都正确
查看答案和解析>>
科目:高中化学 来源: 题型:
选择序号填空:
①16O和18O ②金刚石和石墨 ③CH3CH3和CH3CH2CH2CH3 ④CH3CH2CH2CH3 和CH3CH (CH3) CH3
(1)属于同素异形体的是 ; (2)互为同位素的是 ;
(3)互为同分异构体的是 ; (4)属于同系物的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学──选修2:化学与技术] (15分)
工业上由黄铜矿(主要成分CuFeS2)冶炼铜的主要流程如下:
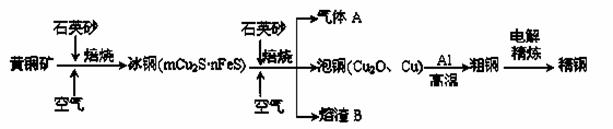
(1)气体A中的大气污染物可选用下列试剂中的_______吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液 d.氨水
(2) ①冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1200℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式是 、______________________________;
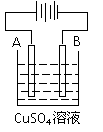 ②熔渣B的主要成分是_______________。
②熔渣B的主要成分是_______________。
(3)由泡铜冶炼粗铜的化学反应方程式为 。
(4)粗铜(含Fe、Ag、Pt、Au等杂质) 的电解精炼如图所示,A极上
发生的反应为__________________________________________,
下列说法正确的是 。
a.电能全部转化为化学能 b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动 d.阴阳两极质量变化相等
(5)利用反应2Cu+O2+2H2SO4=2CuSO4+2H2O可制备CuSO4,若将该反应设计为原电池,
其正极的电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
只用下列试剂中的一种就能将FeCl3、FeCl2、AlCl3和NaCl四种溶液区别开的是( )
A. KSCN溶液 B. BaCl2溶液 C. NaOH溶液 D. AgNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com