
【题目】常温下能盛放在铁制容器中的物质是( )
A.浓盐酸
B.浓硝酸
C.硫酸铜溶液
D.稀硫酸
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源: 题型:
【题目】H2S的分解反应是一个可逆反应,其能量与反应进程的关系如图所示,下列有关说法正确的是( )

A. 正反应的活化能大于逆反应的活化能
B. 若减小体系的压强,则该反应的焓变将增大
C. 升高温度,化学反应速率加快,H2S的平衡转化率减小
D. 向密闭容器中充入1molH2S充分反应,吸收84.9kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s) = Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
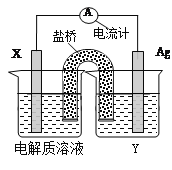
(1)电极X的材料是________;电解质溶液Y是_________;
(2)银电极为电池的________极,发生的电极反应为__________________;X电极上发生的电极反应为________________________;
(3)外电路中的电子是从_______电极流向________电极。
(4)若电极X质量减少6.4g,则Ag极质量增加______ g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表物质按碱、酸、盐、碱性氧化物、酸性氧化物的顺序分类正确的是( )
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | KOH | HCl | NaCl | CaO | CO |
C | NaOH | H2CO3 | CaCl2 | CuO | SO2 |
D | NaOH | HNO3 | BaCO3 | NO | SO3 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中,将一定量A、B气体混合后发生反应:xA(g)+yB(g)![]() zC(g)+mD(s)。平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.3mol/L。则下列有关判断正确的是 ( )
zC(g)+mD(s)。平衡时测得A的浓度为0.5mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.3mol/L。则下列有关判断正确的是 ( )
A. x+y>z+m B. 混合气体的密度一定减小
C. 平衡向正反应方向移动 D. B的转化率一定减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用石油产品A(C4H8),可以合成材料化学重要的物质G和H。己知:
①A和C的核磁共振氢谱都有2组峰,且峰面积之比分别为1∶3和1∶2
②E和F都可发生银镜反应;E的分子式为:C4H4O2
③H2C=CH2+H2O2![]()
![]()
④R-CH2-CHO+HCHO![]()
![]()
G和H的合成路线如下图所示:
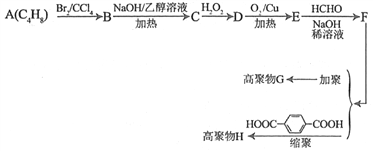
请回答下列问题:
(1)C的名称________________;F中官能团名称为____________________。
(2)A的同分异构体共有___________种(不包括A本身,不含立体异构)
(3)写出B到C的化学方程式和反应类型:
化学方程式为______________________________________________,反应类型是___________。
(4)D→E的化学方程式为___________________________________________。
(5)H的结构简式为_______________________________________________,G的结构简式为____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解足量下列溶液一段时间后,再加入一定量括号内的纯净物,能使溶液恢复到原来的成分和浓度的是
A. AgNO3[AgNO3] B. NaOH[NaOH] C. KCl[H2O] D. CuSO4[CuO]
【答案】D
【解析】石墨电极为惰性电极,溶液中阳离子在阴极放电,阴离子在阳极放电。A、电解AgNO3溶液,Ag+在阴极放电生成Ag,OH-在阳极放电生成O2,且n(Ag)∶n(O2)=2∶1,则应加入Ag2O恢复浓度,故A错误;B、电解NaOH溶液,H+在阴极放电生成H2,OH-在阳极放电生成O2,且n(H2)∶n(O2)=2∶1,则应加入一定量的H2O恢复原样,故B错误;C、电解KCl溶液,H+在阴极放电生成H2,Cl-在阳极放电生成Cl2,且n(H2)∶n(Cl2)=1∶1,则应加入一定量HCl恢复原样,故C错误;D、电解CuSO4溶液,Cu2+在阴极放电生成Cu,OH-在阳极放电生成O2,且n(Cu)∶n(O2)=2∶1,则应加入一定量CuO恢复原样,故D正确。故选D。
点睛:分析电解反应的原理,在两极析出什么物质(固体或气体),相当于什么物质脱离反应体系,根据元素守恒和原子比例,加入对应的物质,即可使溶液完全复原。
【题型】单选题
【结束】
28
【题目】工业上用电解法处理含镍酸性废水并得到单质Ni的原理如图所示。下列说法不正确的是

已知:①Ni2+在弱酸性溶液中发生水解
②氧化性:Ni2+(高浓度)>H+>Ni2+(低浓度)
A. 碳棒上发生的电极反应:4OH--4e-=O2↑+2H2O
B. 电解过程中,B中NaCl溶液的物质的量浓度将不断减少
C. 为了提高Ni的产率,电解过程中需要控制废水pH
D. 若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 丙烯分子中所有原子均在同一平面上
B. ![]() 命名为2-甲基-3-丁炔
命名为2-甲基-3-丁炔
C. 化合物![]() 不是苯的同系物
不是苯的同系物
D. C5H12的同分异构体数目与甲苯的一氯代物数目相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com